حمض نووي
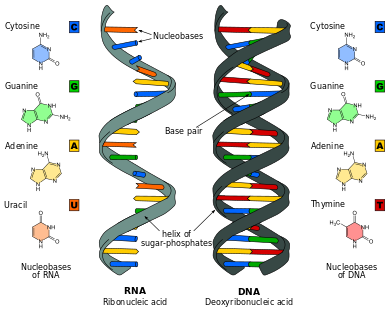
الحَمْض النووي Nucleic acid جزيء معقد موجود في جميع الخلايا. هناك نوعان من الأحماض النووية هما الحمض النووي الريبي منقوص الأكسجين (د. ن. أ) والحمض النووي الريبي (آر. إن. إيه). ويوجد حمض الدنا بصورة رئيسية في نواة الخلية. ولكن (آر. إن. إيه) قد يوجد في جميع أنحاء الخلية. وحتى خلايا البكتيريا التي ليس بها نواة، تحتوي على (د. ن.أ) و (آر. إن. إيه). وهناك فيروسات معينة تحتوي على (آر. إن. إيه) فقط وفيروسات أخرى تحتوي على (د. ن. أ) فقط.
ويؤدي (د. ن. أ) دورًا حيويًا في الوراثة. فهو المادة الرئيسية في الصبغيات (الكروموزومات)، وهي أجسام الخلية التي تنظم عملية الوراثة في الحيوان أو النبات. وعندما تنقسم الخلية يجب أن تنقسم المورثات في نواتها إلى نسخ متطابقة تمامًا تنتقل إلى الخلايا الوليدة. ويقوم (د.ن. أ) الموجود في الصبغيات بإعطاء الخلايا الوليدة مجموعة كاملة من الرموز (الشفرات) من أجل نموها ونمو الخلايا المنحدرة منها.
ويحتوي (د. ن. أ) على الفوسفات، وعلى سكر يسمى الريبوز منقوص الأكسجين، ومركبات تدعى القواعد النيتروجينية. وتكون هذه منظمة في وحدات من فوسفات ـ سكَّر ـ قاعدة ـ فوسفات ـ سكر ـ قاعدة، مكررة مئات الآلاف من المرات لتكون سلسلة طويلة ملتفة. وهذا التركيب الكيميائي الأساسي هو الشائع لكل مركبات (د.ن. أ). ولكن هناك أربع قواعد مختلفة في (د. ن. أ) هي الأدنين والجوانين والثيمين والسيتوسين. والنسب الدقيقة لكل من القواعد، والترتيب الدقيق الذي تُرَتَّب به، تعتبر فريدة لكل نوع من الكائنات الحية. وهذا الترتيب الدقيق وتلك البنية، هما اللذان يجب نسخهما بدقة في كل مرة تنقسم فيها الخلية. وباستطاعة العلماء اصطناع بعض أنواع جزيئات (د. ن. أ) التي باستطاعتها نسخ نفسها.
أما (آر. إن. إيه)، فهو يتكون أيضًا من سلاسل طويلة متكررة من وحدات فوسفات ـ سكر ـ قاعدة. ومع ذلك، فإن السكر في (آر. إن. إيه) هو الريبوز وليس الريبوز منقوص الأكسجين كما هو الحال في (د. ن. أ). والقواعد هي الأدنين، والجوانين، والسيتوسين، واليوراسيل (وليس الثيمين كما هو في (د. ن. أ) ويؤدي (آر. إن. إيه)، دورًا هامًا في تكوين البروتينات.
وبعض جزيئات (آر. إن. إيه)، وتدعى آر. إن. إيه الرسول، تغادر النواة حاملة التعليمات لصنع البروتينات. وتذهب جزيئات (آر. إن. إيه الرسول) هذه إلى الرايبوزومات، وهي تركيبات الخلية التي تصنع فيها البروتينات.
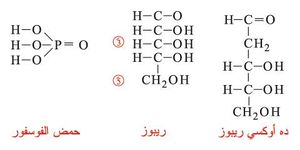
والبروتينات النووية التي تعطي بالإماهة قسماً بروتينياً متجانساً قلوي التفاعل وقسماً لا بروتينياً حامض التفاعل هو الحموض النووية nucleic acides والتي تتواجد في نوى الخلايا الحية وسيتوبلازماها والتي تعطي بالإماهة الكاملة ما يأتي:
ب - سكر بسيط خماسي ذرة الكربون ([[الريبوز أو ده أوكسي ريبوز).
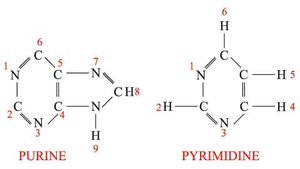
ج - مركبات آزوتية أساسية قلوية التفاعل تدعى قواعد base والتي تنتمي إلى نواة البورين purine أو البيريميدين pyrimidine.
إن القواعد البورية:
1- الآده نين (A) (Adenine) م[6 ـ أمينوبورين]
2- الگوانين (G) (Guanine) م[2 ـ أمينو 6 ـ أوكسي بورين]
,إن القواعد البيريميدية:
1- الأوراسيل (U) (Uracil)م[2 ـ 6 دي أوكسي بيريميدين]
2- التيمين(Thymine) (T) م[5ـ ميتيل أوراسيل]
3- السيتوزين (Cytosine) (C)م[2ـ أوكسي 6ـ أمينو بيريميدين]
الـ نكليوزيد (Nucleoside) والـ نكليوتيد (Nucleotide):
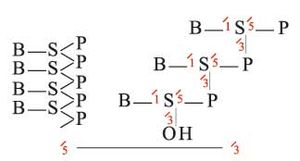
- النكليوزيد: مركب ينجم عن اتحاد جزيء من أس آزوتي (قاعدة) (B) مع جزيء من الـسكر (S) ويرمز لـه بـ (S-B)، إن الارتباط يكون بين ذرة الكربون رقم (1َ) من جزيء السكر مع ذرة الآزوت رقم (3) من جزيء البيريميدين أو رقم (9) من جزيء البورين.
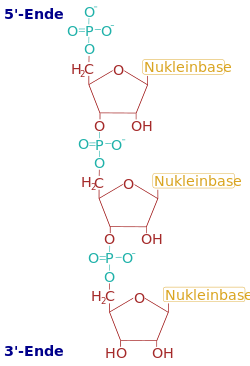
- النكليوتيد: مركب ينجم عن ارتباط جزيء من حمض أورتو الفوسفور مع زمرة هيدروكسيل (OH) الكربون رقم (3َ) أو (5َ) من جزيء السكر في النكليوزيد. إن الأسترة بين حمض الفوسفور والسكر تكون في نفس الوقت على الكربون (3َ) و(5َ) من جزيء السكر في حموض النوى.
تاريخ

Nucleic acid was, partially, first discovered by Friedrich Miescher in 1869 at the University of Tübingen, Germany. He discovered a new substance, which he called nuclein and which - depending on how his results are interpreted in detail - can be seen in modern terms either as a nucleic acid-histone complex or as the actual nucleic acid. Phoebus Levene determined the basic structure of nucleic acids.[2][3][4] In the early 1880s, Albrecht Kossel further purified the nucleid acid substance and discovered its highly acidic properties. He later also identified the nucleobases. In 1889 Richard Altmann created the term nucleic acid – at that time DNA and RNA were not differentiated.[5] In 1938 Astbury and Bell published the first X-ray diffraction pattern of DNA.[6]
In 1944 the Avery–MacLeod–McCarty experiment showed that DNA is the carrier of genetic information and in 1953 Watson and Crick proposed the double-helix structure of DNA.[7]
Experimental studies of nucleic acids constitute a major part of modern biological and medical research, and form a foundation for genome and forensic science, and the biotechnology and pharmaceutical industries.[8][9][10]
التواجد والمسميات
The term nucleic acid is the overall name for DNA and RNA, members of a family of biopolymers,[11] and is a type of polynucleotide. Nucleic acids were named for their initial discovery within the nucleus, and for the presence of phosphate groups (related to phosphoric acid).[12] Although first discovered within the nucleus of eukaryotic cells, nucleic acids are now known to be found in all life forms including within bacteria, archaea, mitochondria, chloroplasts, and viruses (There is debate as to whether viruses are living or non-living). All living cells contain both DNA and RNA (except some cells such as mature red blood cells), while viruses contain either DNA or RNA, but usually not both.[13] The basic component of biological nucleic acids is the nucleotide, each of which contains a pentose sugar (ribose or deoxyribose), a phosphate group, and a nucleobase.[14] Nucleic acids are also generated within the laboratory, through the use of enzymes[15] (DNA and RNA polymerases) and by solid-phase chemical synthesis.
التكوين الجزيئي والحجم
Nucleic acids are generally very large molecules. Indeed, DNA molecules are probably the largest individual molecules known. Well-studied biological nucleic acid molecules range in size from 21 nucleotides (small interfering RNA) to large chromosomes (human chromosome 1 is a single molecule that contains 247 million base pairs[16]).
In most cases, naturally occurring DNA molecules are double-stranded and RNA molecules are single-stranded.[17] There are numerous exceptions, however—some viruses have genomes made of double-stranded RNA and other viruses have single-stranded DNA genomes,[18] and, in some circumstances, nucleic acid structures with three or four strands can form.[19]
Nucleic acids are linear polymers (chains) of nucleotides. Each nucleotide consists of three components: a purine or pyrimidine nucleobase (sometimes termed nitrogenous base or simply base), a pentose sugar, and a phosphate group which makes the molecule acidic. The substructure consisting of a nucleobase plus sugar is termed a nucleoside. Nucleic acid types differ in the structure of the sugar in their nucleotides–DNA contains 2'-deoxyribose while RNA contains ribose (where the only difference is the presence of a hydroxyl group). Also, the nucleobases found in the two nucleic acid types are different: adenine, cytosine, and guanine are found in both RNA and DNA, while thymine occurs in DNA and uracil occurs in RNA.[20]
The sugars and phosphates in nucleic acids are connected to each other in an alternating chain (sugar-phosphate backbone) through phosphodiester linkages.[21] In conventional nomenclature, the carbons to which the phosphate groups attach are the 3'-end and the 5'-end carbons of the sugar. This gives nucleic acids directionality, and the ends of nucleic acid molecules are referred to as 5'-end and 3'-end. The nucleobases are joined to the sugars via an N-glycosidic linkage involving a nucleobase ring nitrogen (N-1 for pyrimidines and N-9 for purines) and the 1' carbon of the pentose sugar ring.
Non-standard nucleosides are also found in both RNA and DNA and usually arise from modification of the standard nucleosides within the DNA molecule or the primary (initial) RNA transcript. Transfer RNA (tRNA) molecules contain a particularly large number of modified nucleosides.[22]
Topology
Double-stranded nucleic acids are made up of complementary sequences, in which extensive Watson-Crick base pairing results in a highly repeated and quite uniform nucleic acid double-helical three-dimensional structure.[23] In contrast, single-stranded RNA and DNA molecules are not constrained to a regular double helix, and can adopt highly complex three-dimensional structures that are based on short stretches of intramolecular base-paired sequences including both Watson-Crick and noncanonical base pairs, and a wide range of complex tertiary interactions.[24]
Nucleic acid molecules are usually unbranched and may occur as linear and circular molecules. For example, bacterial chromosomes, plasmids, mitochondrial DNA, and chloroplast DNA are usually circular double-stranded DNA molecules, while chromosomes of the eukaryotic nucleus are usually linear double-stranded DNA molecules.[13] Most RNA molecules are linear, single-stranded molecules, but both circular and branched molecules can result from RNA splicing reactions.[25] The total amount of pyrimidines in a double-stranded DNA molecule is equal to the total amount of purines. The diameter of the helix is about 20 Å.
التسلسل
One DNA or RNA molecule differs from another primarily in the sequence of nucleotides. Nucleotide sequences are of great importance in biology since they carry the ultimate instructions that encode all biological molecules, molecular assemblies, subcellular and cellular structures, organs, and organisms, and directly enable cognition, memory, and behavior. Enormous efforts have gone into the development of experimental methods to determine the nucleotide sequence of biological DNA and RNA molecules,[26][27] and today hundreds of millions of nucleotides are sequenced daily at genome centers and smaller laboratories worldwide. In addition to maintaining the GenBank nucleic acid sequence database, the National Center for Biotechnology Information (NCBI) provides analysis and retrieval resources for the data in GenBank and other biological data made available through the NCBI web site.[28]
الأنواع
Deoxyribonucleic acid
يوجد نوعان من الأحماض النووية هما:
- الحمض النووي الريبي منقوص الاكسجين (DNA).
- الحمض النووي الريبي (RNA).
التركيب الكيميائي للحامض النووي
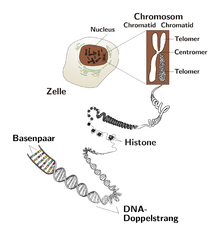
يتركب الحامض النووي من ثلاث أجزاء رئيسية هما:
- مجموعة فوسفات - حمض الفوسفوريك -.
- قواعد نيتروجينية: (السايتوسين و الجوانين و الثايمين و الأدنين و ايضا اليوراسيل في RNA
وهناك نوعان من حموض النوى:
ـ الأول يدعى الحمض النووي الريبي (Ribo Nucleic Acid) (RNA) (رنا).
ـ الثاني يدعى الحمض النووي الريبي المنقوص الأكسجين Deoxyribonucleic Acid) (DNA) (دنا).
إن الفرق بينهما من حيث المكوّنات هو أن:
ـ الرنا لا يحوي على ده أوكسي ريبوز ولا على التيمين.
ـ الدنا لا يحوي على ريبوز ولا على الأوراسيل.
ـ إن الدنا يتواجد في نواة الخلية الحية بكميات كبيرة وفي ميتو كوندريا السيتوبلازما بكميات قليلة.
ـ إن الرنا يتواجد في سيتوبلاسما الخلية بصورة كبيرة وفي نويات النواة بمقادير قليلة.
أ - بنية الرنا:
هو متماثر للنكليوتيدات، وزنه الجزيئي الغرامي بين عشرة آلاف وعدة آلاف ملايين دالتون، تفعل فيه أنزيم الريبونكله آز Ribonuclease وتفككه الى نكليوتيداته.
يتألف جزيء الرنا من طاق واحد Mono - Strand ملتوٍ، وهذا الانطواء يحقق الاتصال بين القواعد. إن هذا الاتصال بين القواعد يتم عن طريق روابط هدروجينية Hydrogen Bond وهناك ثلاث بين (C) و(G) واثنان بين (A) و(U).
إن بنية الطاق يمكن تمثيلها على الشكل الآتي:
هناك عدة أنواع من الرنا أهمها:
1- حمض الرنا المرسال (m RNA) (Messenger RNA)
2- حمض الرنا النقال (t RNA) (Transfer RNA)
3- حمض الرنا الريباسي (r RNA) (Ribosomal RNA)
ب - بنية الدنا:
هو متماثر للنكليوتيدات، وزنه الجزيئي من رتبة مليون دالتون أو أكثر، تفعل فيه أنزيم الده أكسي ريبو نكلياز وتفككه إلى نكليوتيداته Deoxyribonuclease.
لقد تبين أن النسبة تعادل الواحد تقريباً وكذلك النسبة. ونتيجة لبعض الاعتبارات الكيميائية الأخرى افترض واتسون وكريك أن جزيء الدنا مؤلف من سلسلتين خطيتين من النكليوتيدات. وكل من هاتين السلسلتين تشبه سلسلة الرنا من حيث البنية، بمعنى أنه يحوي على طاقين Strands 2 ملتفين على بعضهما على شكل حلزون مضاعف Double Helix. وحيث يكون الاتصال بين القواعد بوساطة روابط هدروجينية [اثنان بين (A) و(T)] و[ثلاث بين (G) و(C)] فإن مسافة اللفة الواحدة في الجزيء تبلغ نحو 3.14 نانومتر وعرضها في حدود 20 نانومتر.
ومن أجل سهولة العرض وفهم آليات عمل الدنا يرمز له على الشكل الآتي:
يدعى الطاق رقم (1) بالطاق المُرمِّز Coding Strand
يدعى الطاق رقم (2) بالطاق المتمِّم Template Strand
ملاحظة: لقد أُعطي للطاق رقم (2) في اللغة العربية أسماء متعددة ونرى دعوته بالمُحسن لأنه هو الطاق الدليل لعملية استنساخ الرنا من الدنا.
إن الصبغيات chromsomes تتكون بصورة أساسية من حمض الدنا DNA. إن عدد الصبغيات في نواة الخلية الحية الإنسانية يبلغ 46 صبغياً تؤلف 23 زوجاً من الصبغيات ويحوي كل زوجين صبغي واحد من الأم وصبغي واحد من الأب. يتألف الصبغي الواحد من [[كروماتيدين Chromatids [[2 متماثلين متصلين ببعضهما بوساطة مايدعى السانترومير Centromer، وكل كروماتيد يحوي جزء من الدنا. إذن هناك 23 صبغياً تأتي من الأم وتدعى هابلوئيد Haploid الأم و23 صبغياً تأتي من الأب وتدعى بـ هابلوئيد الأب .
إن حمض الدنا المتواجد في هابلوئيد الخلية (أي 23 صبغي) يحوي تقريباً على (3.5×10 9) زوجاً من القواعد Base-Pair وهذا ما ندعوه جينوم الهابلوئيد Haploid Genome (ويفضل استخدام كلمة مورثوم بدلاً من جينوم).
إن خيط الدنا DNA في المورثوم يتكون من مناطق تدعى الواحدة منها بالجين Gene (ويفضل استخدام مورثة)، يحوي مورثوم الهابلوئيد في الخلية الإنسانية نحو 1.5 مليون زوجاً من المورثات المتقابلة Allele والتي دعيت بالعربية بالحلائل، والذي لا يعني شيئاً والمفضل تسميتها بالأنداد. إن الأنداد في الصبغي الواحد متماثلة تماماً، أما الأنداد في صبغي الأم وصبغي الأب فقد تكون متماثلة أو غير متماثلة.
Ribonucleic acid
Ribonucleic acid (RNA) functions in converting genetic information from genes into the amino acid sequences of proteins. The three universal types of RNA include transfer RNA (tRNA), messenger RNA (mRNA), and ribosomal RNA (rRNA). Messenger RNA acts to carry genetic sequence information between DNA and ribosomes, directing protein synthesis and carries instructions from DNA in the nucleus to ribosome . Ribosomal RNA reads the DNA sequence, and catalyzes peptide bond formation. Transfer RNA serves as the carrier molecule for amino acids to be used in protein synthesis, and is responsible for decoding the mRNA. In addition, many other classes of RNA are now known.
حمض نووي اصطناعي
Artificial nucleic acid analogues have been designed and synthesized.[29] They include peptide nucleic acid, morpholino- and locked nucleic acid, glycol nucleic acid, and threose nucleic acid. Each of these is distinguished from naturally occurring DNA or RNA by changes to the backbone of the molecules.[citation needed]
الطفرات الصبغية والدنا
إن الأخطاء المرتكبة أثناء اصطناع الدنا وتكاثره واستنساخه في الخلية الحية غالباً ما تصححه الخلية بوساطة أنزيمات خاصة، هناك أخطاء تقع على دنا الصبغي لا يمكن للخلية الحية تصحيحها ويؤدي ذلك إلى ما يدعى طفرات صبغية Chromosomal Mutations. إن هذه الطفرات متعددة ومختلفة وأسبابها أيضاً.
تترجم العضوية الحية صدى هذه الطفرات بحصول اضطرابات استقلابية وبنيوية ناجمة عن تبدل وتغير في بنية الدنا في المورثة وبالتالي تغير وتبدل في التعبير الوراثي Gene Expression.
تشمل هذه الطفرات الصبغية بصورة رئيسية:
أ - طفرة نقطية تنجم عن استبدال نكليوتيد بآخر.
ب - غياب نكليوتيد أو مجموعة من النكليوتيدات.
ت - إدخال نكليوتيد أو مجموعة من النكليوتيدات.
ث - تغير وتبدل في الموضع.
الرنا
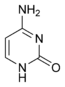 سايتوسين |
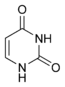 اوراسيل |
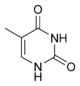 ثايمين |
البيولوجيا الجزيئية Molecular Biology وحموض النوى
في السبعينات من القرن الماضي ظهر مفهوم جديد يدعى البيولوجيا الجزيئية، وهذا المفهوم الذي أصبح علماً قائماً بذاته يهدف إلى دراسة الجزيء الكيميائي الحيوي دراسة دقيقة جداً وربط تبدلات البنية الكيميائية بالأمراض المختلفة الناجمة عن الاضطراب في استقلابه.
إن دراسة بنية حموض النوى وطرق كشفها ومعايرتها وربط ذلك بالأمراض الوراثية وغير الوراثية يكوّن جزءاً هاماً من البيولوجيا الجزيئية يدعى بتقنيات الدنا والرنا DNA & RNA Technology.
المبدأ العملي في كشف حمض نووي ومعايرته
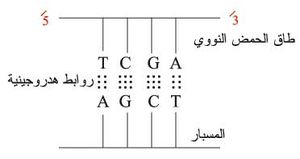
إن المبدأ الرئيسي في ذلك هو استخدام ما يدعى المسبار probe، إن المسبار هو كسرة fragment صغيرة لتسلسل نكليوتيدات ذي طاق وحيد (يحوي على الأقل 15 نكليوتيد).
يجب أن يكون المسبار حاوياً على تسلسل من القواعد قادرة على التقابل والاتصال بما يدعى حالياً بعملية التزاوج hybridization/base-pairing بمعنى أن القاعدة (A) من المسبار تقابل وتتزاوج مع القاعدة (T) أو (U) من طاق الحمض النووي المراد كشفه، وأن القاعدة (G) من المسبار تقابل وتتزاوج مع القاعدة (C) من طاق الحمض النووي المراد كشفه.
إن الشكل الآتي يمثل عملية التزاوج:
إن توافق قواعد المسبار مع قواعد طاق الحمض النووي يمكن كشفها بوسم المسبار labeling من نهايته بوساطة عنصر مشع أو مادة متفلورة أو أنزيم.
إن تقنيات الحموض النووية تشمل بصورة رئيسية:
أ - استخلاص حموض النوى Extraction.
ب - تنقية حموض النوى Purification.
ت - تضخيم وتكثير حموض النوى (التأشيب P.C.R-L.C.R recombination وغيره).
ث - دراسة تسلسل النكليوتيدات في حموض النوى Sequencing.
ج - الرحلان الكهربائي لحموض النوى Electrophoresis.
ح - الرحلان الكهربائي لكسرات حموض النوى بعد تقطيعها بوساطة أنزيمات التقييد والتحديد Ristriction Enzymes. ونقصد بذلك تقنية Southern من أجل الدنا DNA وتقنية Northern من أجل الرنا RNA.
خ - التضخيم وتعيين الهوية بتقنية الأمبليكور Amplicor.
د - تعيين الهوية بتقنية الـ Fish.
ذ - تعيين مكونات الضد وأعمال الطب الشرعي.
ر - تقنية الهندسة الوراثية Genetic Engirneeing.
ز - المعالجة بالمورثات Gene Therapy.
استخلاص وتنقية الحموض النووية
تستخلص الحموض النووية من الخلية الحية بـ:
1- حلّ الخلية Cytolysis.
2- معالجة الحلالة بالفينول.
3- ترسيب الحموض النووية بالغول الإيتيلي أو الإيزو بروبانول.
4- التخلص من الفينول بالإتير.
كما يمكن استخدام بروتوكولات أخرى، وتقوم التقنية على استخدام وسائل متعددة.
تضخيم حموض النوى وتكثيرها
من أجل دراسة حموض النوى من الضروري الحصول على كمية كافية ونقية ما أمكن. ويمكن الحصول على كمية كافية باتباع الطرائق الآتية:
1- في حالة البدء من خلية نسجية أو من خلية فيروسية نقوم بالزرع على أوساط استنباتية خلوية صنعية ومن ثم الاستخلاص.
2- في حالة البدء من خلية جرثومية أو طفيلية نقوم بالزرع على أوساط استنباتية خاصة عادية ومن ثم الاستخلاص.
3- يمكن تضخيم كمية قليلة من الدنا DNA باللجوء إلى ما يدعى التأشيب Recombination.
4- يمكن تضخيم كمية قليلة من الدنا DNA باللجوء إلى ما يدعى الـ PCR أو الـLCR أو الـNASBA
5- يمكن تضخيـم كمية قليلة من الرنا RNA بعد تحويلـها إلى DNA بوساطـة أنزيم (RT) (Reverse Transcriptase).
دراسة تسلسل النكليوتيدات في حموض النوى
الهدف من هذه الدراسة معرفة بنية الحموض النووية بوساطة معرفة تسلسل نكليوتيداتها. ويتم ذلك بحسب منهجين:
أ - منهج SANGER الذي يستخدم ما يدعى 2'-3' Dideoxy Nucleotides.
ب ـ منهج MAXAM الذي يقوم على تخريب النيكليوتيدات C أو G أو T+C أو A+G.
الرحلان الكهربائي لحموض النوى
إن جزيء الحمض النووي مشحون كهربائياً بصورة سلبية بسبب وجود الزمر الحامضة الحرة لحمض الفوسفور.
يُجرى الرحلان على حامل صلب من الآغاروز أو الأكريل أميد في وقاء قلوي (pH=8.6) وبوجود سيالة كهربائية مستمرة.
يمكن إجراء الرحلان على حموض نووية يصل وزنها الجزيئي حتى المليون، كما يمكن إجراء الرحلان على قطع من حموض نووية ندعوها كسرات تحوي من 30 حتى 300 قاعدة.
ومن أجل إظهار المكونات المفرقة نقوم بضغط الحامل الصلب بورق نترات السللوز أو ما شابهه، وبعد انتقال المكونات المفرقة على ورقة نترات السللوز نقوم بغمرها بمسبار مناسب موسوم.
إن المسبار هو تسلسل نكليوتيدي يحوي من 10-15 نكليوتيد على الأقل وقادر على عملية التزاوج أو التتام بصورة نوعية مع المكوّن المفرق. يمكن أن يتم وسم المسبار بوساطة عنصر مشع أو مادة متفلورة أو بأنزيم.
تقنية ساوثرن Southern
هي تقنية خاصة بدراسة الدنا DNA، تشمل ما يأتي:
أ - يقطّع جزيء حمض الدنا ذو الوزن الجزيئي العالي والمستخلص بكميات كبيرة إلى كسرات بوساطة ما يدعى أنزيمات التقييد أو التحديد Restriction Enzymes.
ب - يقطع جزيء الدنا المستخلص بكميات صغيرة إلى كسرات بوساطة أنزيمات التقييد والتحديد ومن ثم يُجرى تضخيمها وتكثيرها بتقنية الـ PCR.
ج - إجراء الرحلان الكهربائي للكسرات.
د - إظهار العصابات المفرقة.
ذ - تطبيق ما سبق على شاهد نظامي.
إن هذه الطريقة مفيدة جداً في دراسة الطفرات على المورثات وتشخيص عدد كبير من الأمراض.
تقنية نورثرن Northern
تقنية مشابهة لتقنية Southern تستخدم في دراسة الرنا RNA.
أنزيمات التقييد والتحديد
أنزيمات من صنف الـ Endo-Nuclease وهي أنزيمات تستخلص بصورة خاصة من الجراثيم ولها أنواع عدة ومختلفة.
إن الأنزيم الواحد قادر على تقطيع سلسلة النكليوتيدات بين قاعدتين معلومتين.
يحوِّل هذا التقطيع حمض النوى إلى كسرات محددة ومعينة، بمعنى أنها تحوي على عدد معلوم من القواعد في الكسرة. وتقدر هذه الكسرات عادة بما يدعى Kb أي ألف قاعدة.
تقنية الأمبليكور Amplicor-Roche
إن هدف هذه التقنية ليس دراسة الطفرات الصبغية وإنما تعيين هوية حمض نووي وعياره.
تشبه هذه التقنية تقنية Southern أو Northern ولكن لا ضرورة هنا لإجراء رحلان كهربائي.
إن هذه التقنية مطبقة حالياً في دراسة عدد كبير من العوامل الممرضة، منها:
4- فيروس الإيدز HIV
5- فيروس CMV
6- عصية السل
… وغير ذلك.
تقنية الـ FISH
تقنية تستخدم من أجل كشف DNA مورثي في صبغي معين.
تقوم هذه الطريقة على تحضير لطاخة نسجية ومسبار مناسب موسوم بمادة متفلورة وباستخدام المجهر التفلوري.
تعيين مكونات الضد وأعمال الطب الشرعي
بما أن مكونات الضد مركبات بروتينية تصنعها الخلية الحية بوساطة ريباساتها وبإشراف الرنا المرسال mRNA المستنسخ عن المورثة الخاصة بها، فإنه من الأفضل تعيين هوية هذه المكونات الضدية ليس بكشفها بصورة مباشرة بأضدادها، وإنما بدراسة المورثات التي تعبر عنها، ويفيد ذلك في:
أ - تعيين زمر الكريات الحمراء.
ب - تعيين زمر الـHLA للكريات البيضاء.
ج - كشف العوز في الأنزيمات.
د - كشف الطفرات الصبغية.
ذ - اختبارات تعيين الهوية وتحديد الأبوة والبنوة.
ر - دراسة التسلسل العرقي.
ز - تعيين هوية البقايا البشرية.
ح - الفصل في الحوادث الإجرامية.
ط - حل مشاكل التأمين.
تقنية الهندسة الوراثية
هي تقنية تقوم على نقل مورثة (قطعة من الدنا DNA) من خلية حية نظامية ترمز لمركب كيميائي محدد ومعين إلى خلية جرثومية مضيافة بوساطة عملية التأشيب.
تصبح الخلية الجرثومية المضيافة قادرة على صنع المركب الكيميائي من ضمن المركبات التي تصنعها أصلاً، ولقد أمكن بوساطة هذه التقنية الحصول على مركبات صنعية حيوية عديدة ومختلفة نذكر منها:
هرمون الأنسولين الإنساني وهرمون الهوموبويه تين.
المعالجة بالمورثات
هي استراتيجية هامة الهدف منها معالجة الأمراض الوراثية، وذلك بنقل مورثة نظامية من خلية حية إلى خلية مريضة كانت قد فقدت المورثة أو حصل على هذه المورثة اضطراب ما.
إن بروتوكولات هذه المعالجة متعددة ومختلفة ومعقدة ولا تزال في مراحلها الأولية ولكن المستقبل واعد.
تشخيص فاقة الدم المنجلية
نعطي في تشخيص هذا المرض فكرة عن تطبيق تقنية الدنا DNA.
يمكن أن يحوي الخضاب الدموي Hb المستخلص من الكريات الحمراء للمريض:
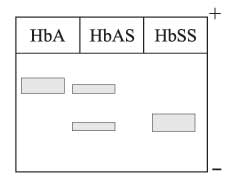
1- الخضاب الكهلي النظامي HbA ممزوجاً مع الخضاب المنجلي HbS، ويصادف ذلك في المرضى متخالفي الإلقاح heterozygot ويمكن إعطاء هذا المزيج الرمز HbAS.
2- الخضاب المنجلي HbS فقط، ويصادف ذلك في المرضى متجانسي الإلقاح hemozygot
ويمكن أن يرمز للخضاب في هذه الحالة بـ HbSS.
يختلف الخضاب (HbS) عن الخضاب الكهلي (HbA) بأن السلسلة الغلوبينية بيتا β تحوي الحمض الأميني المدعو valine في الموضع (6) بدل الحمض الأميني المدعو Glutamic acid في الخضاب HbA ومن أجل تشخيص هذا الداء يُعمد إلى الخطوات الآتية:
أ - تُعزل المورثة المرمزة للسلسلة الغلوبينية β من خلية منواة (ليس من الكريات الحمراء وليس من الصفيحات) ويمكن أن تكون هذه الخلية مأخوذة من الجنين بطريقة مناسبة، ومن ثم يستخلص الدنا منها.
ب - يُقطّع حمض النوى المعزول إلى كسرات بوساطة أنزيمات تحديد وتقييد خاصة أو تكثير هذه الكسرات بتقنية الـPCR.
ت - يُجرى رحلان كهربائي للكسرات على هلامة الآغار.
ث - تُظهر العصابات المفرقة على هلامة الآغار بوساطة مسبار خاص.
ج - يُعمل شاهد مراقبة من مورثة نظامية.[30]
ح - تكون النتائج على الشكل الآتي:
المصادر
- Keith Roberts, Martin Raff, Bruce Alberts, Peter Walter, Julian Lewis and Alexander Johnson, Molecular Biology of the Cell 4th Edition, Routledge, March, 2002, hardcover, 1616 pages, 7.6 pounds, ISBN 0-8153-3218-1
انظر أيضاً
- Comparison of nucleic acid simulation software
- History of biochemistry
- تاريخ علم الأحياء الجزيئي
- History of RNA biology
- Molecular biology
- Nucleic acid methods
- Nucleic acid metabolism
- Nucleic acid structure
- Nucleic acid thermodynamics
- Oligonucleotide synthesis
- Quantification of nucleic acids
المراجع
- ^ Bill Bryson, A Short History of Nearly Everything, Broadway Books, 2015.p. 500.
- ^ Bannwarth, Horst. "Lexikon der Biologie". Spektrum.de (in الألمانية). Retrieved 2024-06-24.
- ^ Dahm R (January 2008). "Discovering DNA: Friedrich Miescher and the early years of nucleic acid research". Human Genetics. 122 (6): 565–581. doi:10.1007/s00439-007-0433-0. PMID 17901982. S2CID 915930. (Note: Page 575 mentions the inclusion or non-inclusion of proteins (histons) in the nuclein concept)
- ^ Edlbacher, S. (2020). Kurzgefasstes Lehrbuch der physiologischen Chemie (in الألمانية). De Gruyter. p. 85. ISBN 978-3-11-146382-7. Retrieved 2024-06-24. (Note: The original text is from 1940)
- ^ "BIOdotEDU". www.brooklyn.cuny.edu. Retrieved 1 January 2022.
- ^ Cox M, Nelson D (2008). Principles of Biochemistry. Susan Winslow. p. 288. ISBN 9781464163074.
- ^ "DNA Structure". What is DNA. Linda Clarks. Archived from the original on August 3, 2016. Retrieved 6 August 2016.
{{cite web}}: CS1 maint: unfit URL (link) - ^ Lander ES, Linton LM, Birren B, Nusbaum C, Zody MC, Baldwin J, et al. (February 2001). "Initial sequencing and analysis of the human genome" (PDF). Nature. 409 (6822): 860–921. Bibcode:2001Natur.409..860L. doi:10.1038/35057062. PMID 11237011.
- ^ Venter JC, Adams MD, Myers EW, Li PW, Mural RJ, Sutton GG, et al. (February 2001). "The sequence of the human genome". Science. 291 (5507): 1304–51. Bibcode:2001Sci...291.1304V. doi:10.1126/science.1058040. PMID 11181995.
- ^ Budowle B, van Daal A (April 2009). "Extracting evidence from forensic DNA analyses: future molecular biology directions". BioTechniques. 46 (5): 339–40, 342–50. doi:10.2144/000113136. PMID 19480629.
- ^ Elson D (1965). "Metabolism of Nucleic Acids (Macromolecular DNA and RNA)". Annual Review of Biochemistry. 34: 449–86. doi:10.1146/annurev.bi.34.070165.002313. PMID 14321176.
- ^ Dahm R (January 2008). "Discovering DNA: Friedrich Miescher and the early years of nucleic acid research". Human Genetics. nih.gov. 122 (6): 565–81. doi:10.1007/s00439-007-0433-0. PMID 17901982. S2CID 915930.
- ^ أ ب Brock TD, Madigan MT (2009). Brock biology of microorganisms. Pearson / Benjamin Cummings. ISBN 978-0-321-53615-0.
- ^ Hardinger, Steven; University of California, Los Angeles (2011). "Knowing Nucleic Acids" (PDF). ucla.edu.
- ^ Mullis, Kary B. The Polymerase Chain Reaction (Nobel Lecture). 1993. (retrieved December 1, 2010) http://nobelprize.org/nobel_prizes/chemistry/laureates/1993/mullis-lecture.html
- ^ Gregory SG, Barlow KF, McLay KE, Kaul R, Swarbreck D, Dunham A, et al. (May 2006). "The DNA sequence and biological annotation of human chromosome 1". Nature. 441 (7091): 315–21. Bibcode:2006Natur.441..315G. doi:10.1038/nature04727. PMID 16710414.
- ^ Todorov TI, Morris MD (April 2002). National Institutes of Health. "Comparison of RNA, single-stranded DNA and double-stranded DNA behavior during capillary electrophoresis in semidilute polymer solutions". Electrophoresis. nih.gov. 23 (7–8): 1033–44. doi:10.1002/1522-2683(200204)23:7/8<1033::AID-ELPS1033>3.0.CO;2-7. PMID 11981850. S2CID 33167686.
- ^ Margaret Hunt; University of South Carolina (2010). "RN Virus Replication Strategies". sc.edu.
- ^ McGlynn P, Lloyd RG (August 1999). "RecG helicase activity at three- and four-strand DNA structures". Nucleic Acids Research. 27 (15): 3049–56. doi:10.1093/nar/27.15.3049. PMC 148529. PMID 10454599.
- ^ Zedalis, Julianne; Eggebrecht, John (2018-03-08). "14.2 DNA Structure and Sequencing - Biology for AP® Courses | OpenStax". openstax.org (in English). Retrieved 2025-11-17.
{{cite web}}: CS1 maint: unrecognized language (link) - ^ Stryer, Lubert; Berg, Jeremy Mark; Tymoczko, John L. (2007). Biochemistry. San Francisco: W.H. Freeman. ISBN 978-0-7167-6766-4.
- ^ Rich A, RajBhandary UL (1976). "Transfer RNA: molecular structure, sequence, and properties". Annual Review of Biochemistry. 45 (1): 805–60. Bibcode:1976ARBio..45..805R. doi:10.1146/annurev.bi.45.070176.004105. PMID 60910.
- ^ Watson JD, Crick FH (April 1953). "Molecular structure of nucleic acids; a structure for deoxyribose nucleic acid". Nature. 171 (4356): 737–8. Bibcode:1953Natur.171..737W. doi:10.1038/171737a0. PMID 13054692. S2CID 4253007.
- ^ Ferré-D'Amaré AR, Doudna JA (1999). "RNA folds: insights from recent crystal structures". Annual Review of Biophysics and Biomolecular Structure. 28: 57–73. doi:10.1146/annurev.biophys.28.1.57. PMID 10410795.
- ^ Alberts, Bruce (2008). Molecular biology of the cell. New York: Garland Science. ISBN 978-0-8153-4105-5.
- ^ Gilbert, Walter G. 1980. DNA Sequencing and Gene Structure (Nobel Lecture) http://nobelprize.org/nobel_prizes/chemistry/laureates/1980/gilbert-lecture.html
- ^ Sanger, Frederick. 1980. Determination of Nucleotide Sequences in DNA (Nobel Lecture) http://nobelprize.org/nobel_prizes/chemistry/laureates/1980/sanger-lecture.html
- ^ NCBI Resource Coordinators (January 2014). "Database resources of the National Center for Biotechnology Information". Nucleic Acids Research. 42 (Database issue): D7-17. doi:10.1093/nar/gkt1146. PMC 3965057. PMID 24259429.
- ^ Sandeep Verma; Fritz Eckstein (1998). "Modified Oligonucleotides: Synthesis and Strategy for Users". Annual Review of Biochemistry. 67: 99–134. doi:10.1146/annurev.biochem.67.1.99. PMID 9759484.
{{cite journal}}: Check|author-link2=value (help) - ^ محمود دلول. "الحموض النووية". الموسوعة العربية.
ببليوجرافيا
- Wolfram Saenger, Principles of Nucleic Acid Structure, 1984, Springer-Verlag New York Inc.
- Bruce Alberts, Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, and Peter Walter Molecular Biology of the Cell, 2007, ISBN 978-0-8153-4105-5. Fourth edition is available online through the NCBI Bookshelf: link
- Jeremy M Berg, John L Tymoczko, and Lubert Stryer, Biochemistry 5th edition, 2002, W H Freeman. Available online through the NCBI Bookshelf: link
- Astrid Sigel; Helmut Sigel; Roland K. O. Sigel, eds. (2012). Interplay between Metal Ions and Nucleic Acids. Metal Ions in Life Sciences. Vol. 10. Springer. doi:10.1007/978-94-007-2172-2. ISBN 978-94-007-2171-5. S2CID 92951134.
للاستزادة
- Palou-Mir J, Barceló-Oliver M, Sigel RK (2017). "Chapter 12. The Role of Lead(II) in Nucleic Acids". In Astrid S, Helmut S, Sigel RK (eds.). Lead: Its Effects on Environment and Health. Metal Ions in Life Sciences. Vol. 17. de Gruyter. pp. 403–434. doi:10.1515/9783110434330-012. PMID 28731305.
وصلات خارجية
- Interview with Aaron Klug, Nobel Laureate for structural elucidation of biologically important nucleic-acid protein complexes provided by the Vega Science Trust.
- Nucleic Acids Research journal
- Nucleic Acids Book (free online book on the chemistry and biology of nucleic acids)
- Visualization of nucleotide sequence