الجهاز العصبي المعوي
الدماغ الثاني ... في أمعائنا
| د.إيهاب عبد الرحيم محمد ساهم بشكل رئيسي في تحرير هذا المقال
|
| Enteric nervous system | |
|---|---|
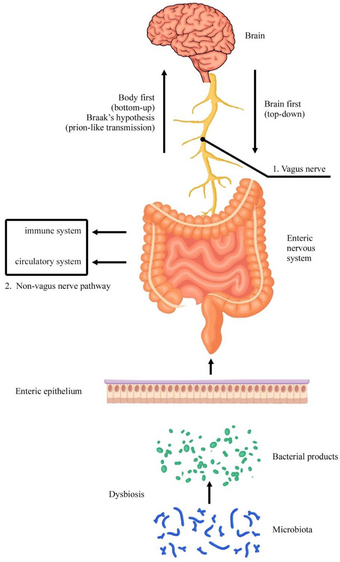 The enteric nervous system is embedded in the lining of the gastrointestinal system. | |
| المرادفات | intrinsic nervous system |
| المُعرفات | |
| الاختصارات | ENS |
| MeSH | D017615 |
| FMA | 66070 |
| المصطلحات التشريحية | |
الجهاز العصبي المعوي (ENS) هو واحد من ثلاثةأقسام في autonomic nervous system (ANS), the others being the sympathetic nervous system (SNS) and parasympathetic nervous system (PSNS). It consists of a mesh-like system of neurons that governs the function of the gastrointestinal tract.[1] The ENS is nicknamed the "second brain".[2][3] It is derived from neural crest cells.[4][5]
The enteric nervous system is capable of operating independently of the brain and spinal cord,[6] but is thought to rely on innervation from the vagus nerve and prevertebral ganglia in healthy subjects. However, studies have shown that the system is operable with a severed vagus nerve.[7] The neurons of the enteric nervous system control the motor functions of the system, in addition to the secretion of gastrointestinal enzymes. These neurons communicate through many neurotransmitters similar to the CNS, including acetylcholine, dopamine, and serotonin. The large presence of serotonin and dopamine in the intestines are key areas of research for neurogastroenterology.[8][9][10]
في أعماق أحشائك، تقبع ذات حركية معقدة- وهي جهاز عصبي كامل يحتوي على خلايا عصبية أكثر من تلك التي يضمها الحبل الشوكي، بل وأكثر من الخلايا التي يحتوي عليها بقية الجهاز العصبي الطرفي- هناك أكثر من 100 مليون خلية عصبية في الأمعاء الدقيقة وحدها! على الرغم من أن البعض كانوا يعتبرونه مجرد تجمع بسيط من العقد العصبية، يعرف الجهاز العصبي المعوي (Enteric Nervous System; ENS) حاليا لكونه دماغا ثانيا مستقلا بذاته. وبرغم أننا لا نزال غير قادرين على الربط بين السلوكيات المعقدة مثل حركة الأمعاء والإفرازات المعوية، وبين خلايا عصبية محددة، إلا أن الأبحاث الجارية في هذا المجال تتقدم بسرعة هائلة، مما سيؤدي لحدوث تطورات مهمة في تدبير الأمراض الوظيفية للأمعاء.
من الناحيتين التركيبية والكيميائية، يعد الجهاز العصبي المعوي دماغا بحد ذاته، فبين تلافيف الأمعاء التي يبلغ طولها عدة أمتار، تقبع شبكة معقدة من الخلايا العصبية التي يتحكم في أنشطتها عدد من الناقلات العصبية Neurotransmitters والمعدِّلات العصبية Neuromodulators ، أكبر بكثير مما يوجد في أي مكان آخر من الجهاز العصبي الطرفي، مما يسمح للجهاز العصبي المعوي بممارسة أنشطته بصورة مستقلة عن الجهاز العصبي المركزي- وهي صفة فريدة أتاحت لعلماء البيولوجيا العصبية المعوية دراسة تطور الخلايا العصبية والوسائط الكيميائية للسلوك المنعكس داخل بيئة المختبر، مما أدى لظهور فرع علمي مستقل هو طب أعصاب الجهاز الهضمي Neurogastroenterology.
البنية

The enteric nervous system in humans consists of some 500 million neurons[11] (including the various types of Dogiel cells),[1][12] 0.5% of the number of neurons in the brain, five times as many as the one hundred million neurons in the human spinal cord,[13] and about 2⁄3 as many as in the whole nervous system of a cat. The enteric nervous system is embedded in the lining of the gastrointestinal system, beginning in the esophagus and extending down to the anus.[13]
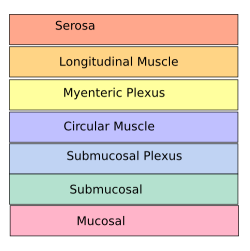
The neurons of the ENS are collected into two types of ganglia: myenteric (Auerbach's) and submucosal (Meissner's) plexuses.[14] Myenteric plexuses are located between the inner and outer layers of the muscularis externa, while submucosal plexuses are located in the submucosa.
Auerbach's plexus
Auerbach's plexus, also known as the myenteric plexus, is a collection of fibers and postganglionic autonomic cell bodies that lie between the circular and longitudinal layers of the muscularis externa in the gastrointestinal tract.[citation needed] It was discovered and named by German neuropathologist Leopold Auerbach. These neurons provide motor inputs to both layers of the muscularis externa and provide both parasympathetic and sympathetic input. The anatomy of the plexus is similar to the anatomy of the central nervous system. The plexus includes sensory receptors, such as chemoreceptors and mechanoreceptors, that are used to provide sensory input to the interneurons in the enteric nervous system. The plexus is the parasympathetic nucleus of origin for the vagus nerve and communicates with the medulla oblongata through both the anterior and posterior vagal nerves.
Submucosal plexus
The submucosal plexus (also known as Meissner's plexus) is found in the submucosal layer of the gastrointestinal tract.[15] It was discovered and named by German physiologist Georg Meissner. It functions as a pathway for the innervation in the mucosa layer of the gastrointestinal wall.
تاريخ
يرجع البحث في طب أعصاب الجهاز الهضمي للقرن التاسع عشر، حيث أظهر الباحثان البريطانيان وليام بايلس Bayliss وإرنست ستارلنج Starling أن الضغط على تجويف البطن في الكلاب المخدَّرَة يؤدي إلى انقباض الفم وارتخاء الشرج، يليها حدوث موجة دافعة (وهو ما أطلق عليه وقتها اسم "قانون الأمعاء"، ويعرف الآن باسم منعكس التمعج Peristaltic reflex) ، بقوة تكفي لدفع الطعام عبر السبيل الهضمي. ونظرا لأن هذا المنعكس يظل فاعلا حتى بعد قطع الأعصاب الخارجية الواصلة إلى الأمعاء. وقد استنتج بايلس وستارلنج – محقين- أن الجهاز العصبي المعوي عبارة عن محور ذاتي من النشاط العصبي يعمل بصورة مستقلة بدرجة كبيرة عن الجهاز العصبي المركزي. وبعد ذلك بثمانية عشر عاما، أثبت العالم الألماني فريدرش ترندلنبورج Friedrich Trendelenburg صحة هذه الاكتشافات بإظهار إمكانية إحداث منعكس التمعج خارج الجسم الحي في الأمعاء المعزولة لحيوانات التجارب، دون مشاركة من الدماغ، أو الحبل الشوكي، أو العقد القحفية. كان ترندلنبرج على علم بأن هذه الاكتشافات فريدة من نوعها؛ فليس هناك عضو طرفي آخر يمتلك مثل هذا الجهاز العصبي الداخلي المعقد؛ فإذا تم قطع الاتصالات العصبية بين الدماغ وبين المثانة أو العضلات الهيكلية على سبيل المثال، فستتوقف جميع الأنشطة الحركية لهذه الأعضاء؛ أما إذا تم قطع الاتصالات العصبية إلى الأمعاء، فستظل وظيفتها كما هي دون تغير.
تم نشر أبحاث ترندلنبرج عام 1917، ويبدو أن هناك عددا من معاصريه كانوا يشاركونه الرأي، كما يتضح من وصف الجهاز العصبي المعوي داخل كتاب جون لانجلي Langley الكلاسيكي عن الجهاز العصبي المستقل، والمنشور عام 1921. وقد توقع لانجلي أن هناك الملايين من الخلايا العصبية في الأمعاء، وأنها تؤلف أحد الأجزاء الثلاثة التي وضعها للجهاز العصبي المستقل؛ الودي (السمبتاوي)، واللاودي (الباراسمبتاوي)، والمعوي. كان لانجلي صاحب ومحرر المجلة الفيزيولوجية (مجلة علم وظائف الأعضاء)، ولسوء الحظ فقد كانت علاقته سيئة بالكثيرين من زملائه. ولذلك، فبعد وفاته، قامت هيئة التحرير الجديدة للمجلة الفيزيولوجية بإعادة تصنيف العصبونات المعوية Enteric neurons على أنها جزء من الإمداد العصبي للعصب الحائر (المبهم vagus)، والذي يتحكم في حركة الأمعاء. وبرغم أن هذا التصنيف صحيح إلى حد ما، إلى أنه أدى إلى إهمال مفهوم وجود جهاز عصبي معوي مستقل- فقد انشغل الباحثون بمتابعة التطورات المتلاحقة في مجال الناقلات العصبية؛ حيث تم التعرف على الإبينفرين epinephrine والأستيل كولين acetylcholine كناقلات عصبية في الجهازين السمبتاوي والباراسمبتاوي (برغم أن النقال العصبي الفعلي للجهاز السبمتاوي قد اكتشف لاحقا أنه النور إبينفرين). وقد ظلت هذه النظرية سائدة حتى عام 1965، عندما أثبت الباحث الأمريكي مايكل جيرشون Gershon وجود ناقل عصبي ثالث، وهو السيروتونين؛ يستهدف الجهاز العصبي المعوي.
ولتجدد الاهتمام بالجهاز العصبي المعوي جذور تاريخية قوية، فمنذ ما يقرب من 100 عام، أجرى الطبيب الأمريكي بايرون روبنسون Robinson أبحاثا متعمقة عن الموضوع، ضَمَّنَها كتابه المثير للإعجاب بعنوان "الدماغ البطني والحوضي"، والمنشور عام 1907. ويخلص كتاب روبنسون هذا إلى أن الأحشاء البطنية تحتوي على جهاز عصبي هائل ومعقد، يقوم بالتحكم وتنظيم العمليات الحيوية للأحشاء البطنية. ولم يكن روبنسون و لانجلي وحيدين في اهتمامهما بالجهاز العصبي للبطن، فقد كان إدجار كايس Cayce، والذي أطلق عليه اسم أبو الطب الشمولي ، من كبار المتحمسين لفكرة وجود جهاز عصبي بطني مستقل. كان كايس يعتقد بأن الأنماط "المجهولة المنشأ" من بعض المتلازمات العصبية ، مثل الصَرَع والشقيقة (الصداع النصفي)، تنتج عن أسباب بطنية. وقد اقترح كايس عددا كبيرا من المعالجات الطبيعية لهذه المتلازمات.
الدماغ الثاني…كيف تفكر الأمعاء؟
يبدو الهضم عملية مألوفة لدرجة أن أغلب الناس يفضلون عدم التفكير فيها. ولحسن الحظ، فليس عليهم أن يفكروا بذلك- على الأقل باستخدام أدمغتهم التي في رؤوسهم! وبرغم أن قليلين على علم بذلك، فالبشر (والحيوانات الأخرى) يمتلكون دماغا ثانيا يتحكم في أغلب الوظائف الهضمية. في أعماق أحشائك، تقبع ذات حركية معقدة- وهي جهاز عصبي كامل يحتوي على خلايا عصبية أكثر من تلك التي يضمها الحبل الشوكي، بل وأكثر من الخلايا التي يحتوي عليها بقية الجهاز العصبي الطرفي- هناك أكثر من 100 مليون خلية عصبية في الأمعاء الدقيقة وحدها! قد تسهم اضطرابات "الدماغ المعوي" هذا في حدوث متلازمة القولون العصبي ، وهي حالة مرضية تصيب نحو 20 % من سكان البلدان الصناعية، ويعتقد أنها مسؤولة عن خسائر تقدر بنحو 8 مليار دولار من أموال الرعاية الصحية سنويا في الولايات المتحدة وحدها. ويعاني ضحايا هذا المرض من نوبات من الإسهال أو الإمساك المزمن أو كليهما بالتبادل في بعض الأحيان. ويعد تشخيص القولون العصبي أكثر تشخيص يتوصل إليه أطباء الجهاز الهضمي. إن وظيفة الجهاز الهضمي معقدة للغاية، فإذا كان على الدماغ أن يتحكم فيها، لتوجب عليه أن يخصص عددا هائلا من الخلايا العصبية لهذا الغرض وحده؛ ولذلك يرى العلماء أن وظيفة الجهاز العصبي المعوي مستقلة عن الجهاز العصبي المركزي. وعلى الرغم من ذلك، فمن الممكن أن يؤثر الجهاز العصبي المعوي على الجهاز العصبي المركزي عن طريق كل من المنعكسات العصبية neurological reflexes والببتيدات العصبية neuropeptides. ويقدر الباحثون أن 80% من ألياف العصب المبهم تعد واردات حشوية visceral afferents، وأظهرت الأبحاث الحديثة وجود تراكب هائل بين نشاط الببتيدات العصبية في كل من الأمعاء والدماغ. ويعد الجهاز العصبي المعوي مجالا خصبا للأبحاث حاليا، حيث نشرت أكثر من 600 مقالة علمية في الموضوع منذ عام 1985!
الصَرَع البطني:
تم التعرف على وجود ارتباط بين الأعراض البطنية وبين الصَرَع epilepsy منذ زمن بعيد؛ فعلى سبيل المثال، كانت "الاضطرابات المعدية والمعوية" ينظر إليها كعوامل سببية رئيسية من قبل الأطباء في القرن التاسع عشر وأوائل القرن العشرين. وتعد الأورة aura مثالا آخر على الارتباط البطني للصَرَع، وهي شائعة في بعض أنواع الصَرَع ، فنوبات صَرَع الفص الصدغي تبدأ بالأورة. ومن وجهة نظر طب الأعصاب، فهذه الأورة هي في الواقع نوبة خفيفة تسبق النوبة الصَرَعية الأولية، ويمكن اعتبارها تحذيرا بقرب حدوث النوبة. وفي أغلب الأحيان، تظهر الأورة في صورة اضطراب مبهم في المعدة وينتقل إلى الصدر. وقد أعاد الطب الحديث اكتشاف الصلة بين الصَرَع وبين البطن، وهناك عدد قليل من الأبحاث التي نشرت في الستينات من القرن العشرين، والتي لفتت الأنظار إلى الملامح البطنية المتعلقة بالصَرَع. وخلال السنوات الخمس والعشرين الأخيرة، ذكرت تقارير كثير من الأطباء الممارسين الجوانب المتعددة للصَرَع البطني، والتي تشمل: ألم البطن، والغثيان، والانتفاخ، والإسهال؛ مع مظاهر متعلقة بالجهاز العصبي المركزي مثل الصداع، والتخليط، والإغماء. وعلى الرغم من أن الأعراض البطنية قد تتشابه مع تلك الموجودة في حالة القولون العصبي، إلا أنه من الممكن التفريق بينهما بوجود بعض التغير في مستوى الوعي أثناء النوبة، مع تغيرات شاذة في تخطيط كهربية الدماغ (EEG). ومن أهم المشكلات التي تواجهنا في محاولتنا لفهم الصَرَع البطني، نجد التحديد الدقيق للعلاقة بين الأعراض البطنية وبين النشاط العصبي الشاذ في الدماغ. كما تلقى دور العصب المبهم اهتماما خاصا يتمثل في إجراء جراحي يتم فيه زراعة ناظمة pacemaker في العصب المبهم بأعلى الصدر. وقد أدى التنبيه المنتظم للعصب المبهم بواسطة الناظمة إلى تقليل أو إزالة الاختلاجات في بعض المرضى المستعصين على العلاج. فإذا كان تنبيه الجهاز العصبي الطرفي، ممثلا في هذه الحالة بالعصب المبهم، يمكنه تقليل النشاط العصبي الشاذ في الدماغ، فربما كانت الاستثارة المرضية لهذا العصب ، أو غيره من الأعصاب الطرفية، تلعب دورا في سببيات بعض أنواع الصَرَع.
الشقيقة البطنية
من وجهة النظر الطبية، تظهر الشقيقة (الصداع النصفي: migraine) كمرض جهازي مركب، يظهر على هيئة توليفات متباينة من الأعراض العصبية، والهضمية ، والمستقلة (الأوتونومية). وبرغم أن المكونات العصبية تستأثر بمعظم الاهتمام في التشخيص والعلاج الطبي، فإن وجهات النظر التاريخية- والمعاصرة أحيانا- تخلع على الأعراض الهضمية مكانة مميزة. ويميل المنظور التاريخي لمتلازمة مثل الشقيقة لوضع جميع الأعراض في الاعتبار نحو تفسير أكثر شمولا للمرض. ولذلك، فقد تلقت الملامح الهضمية الرئيسية للشقيقة اهتماما أكثر بكثير، فيما يتعلق بكل من السببيات والعلاج. وقد ركزت معالجات الشقيقة في الماضي على الملامح الهضمية مباشرة ، من خلال مجموعة كبيرة من المعالجات شبه الطبيعية بهدف تحسين وظائف الهضم، والتمثيل الغذائي، والإخراج عبر الأمعاء.
أما العلوم الطبية الحديثة ، فقد اعترفت بإعادة اكتشاف الارتباط البطني بالشقيقة بعدة صور؛ أهمها الاعتراف بوجود صورة إكلينيكية مستقلة، أطلق عليها اسم "الشقيقة البطنية" abdominal migraine ، والتي يتم تشخيصها في الأطفال أكثر من الكبار. وقد خلصت الأبحاث المتعددة التي أجريت بهذا الخصوص إلى وجود أدلة مؤكدة على أن الألم البطني المتكرر يعد واحدا من الملامح المبكرة للشقيقة، ويدعم بقوة وجود ارتباط سببي بين الألم البطني الراجع recurrent وبين الشقيقة. وقد اكتشفت العلاقة بين الجهاز الهضمي والشقيقة أيضا في صورة حساسية لبعض أنواع الأغذية؛ فكان المتخصصون في الحساسية يرون أن التعب، والعوامل العصبية والعاطفية، تحدث تغيرات في الأنشطة الحركية للجهاز الهضمي، مما يؤدي لركود الطعام في الاثنا عشري duodenum. ويؤدي ذلك لتشجيع امتصاص مولدات الحساسية ، ويستجيب الجسم لذلك بالشعور بالصداع النصفي (الشقيقة). ويذكر أولئك العلماء أن الأنظمة الغذائية الخاصة بالحساسية تؤدي إلى شفاء 5% من المرضى، وإلى تحسن جزئي في 45% من المصابين بالشقيقة.
التوحد ذو الملامح المعوية:
يظهر المصابون بالتوحد autism ثلاثة أنواع من الأعراض؛ تعطل التفاعل مع المجتمع ، ومشكلات متعلقة بالتواصل والتخيل اللفظي وغير اللفظي، ووجود أنشطة واهتمامات شاذة أو محدودة للغاية. وعادة ما تظهر أعراض التوحد خلال السنوات الثلاث الأولى من العمر، وتستمر طوال الحياة. وعلى الرغم من أن هذا المرض لا علاج له حتى الآن، إلا أن التدبير المناسب له قد يساعد على النمو الطبيعي للطفل، ويقلل من السلوكيات غير المرغوب فيها. وقد أضافت الأبحاث الطبية الحديثة مرض التوحد إلى القائمة المتنامية دوما للأمراض العصبية ذات الملامح البطنية؛ حيث تؤكد تلك الأبحاث على وجود نمط مميز من التهاب الأمعاء في نسبة كبيرة من الأطفال المصابين بالتوحد . وقد يؤدي فهم العلاقة بين الأمعاء وبين الدماغ في مرضى التوحد إلى مزيد من الفهم لهذا المرض المعوِّق. وقد ظهرت أدلة جديدة على دور العامل المعوي في مرضى التوحد، عندما وجد أن مادة السيكريتين secretin فعالة بصورة مدهشة في علاج التوحد لدى بعض الأطفال؛ وهي مادة طبيعية يفرزها الجهاز الهضمي لجميع الثدييات. وعادة ما يتم إعطاء السيكريتين عن طريق الحقن الوريدي البطيء، وهو ما يعرف بالتسريب infusion. وقد حصلت هذه المادة على موافقة هيئة الأغذية والأدوية FDA ، وهي الجهة المسؤولة عن منح التراخيص للأدوية الجديدة في الولايات المتحدة، وذلك لعلاج الاضطرابات الهضمية، على أنها تعتبر علاجا لا يجوز صرفه إلا بموجب وصفة طبية.
Function
The ENS is capable of autonomous functions[16] like the coordination of reflexes; although it receives considerable innervation from the autonomic nervous system, it can and does operate independently of the brain and the spinal cord.[17] Its study is the focus of neurogastroenterology.
Complexity
The enteric nervous system is a complex part of the nervous system. The enteric nervous system can operate autonomously. It normally communicates with the central nervous system (CNS) through the parasympathetic (e.g., via the vagus nerve) and sympathetic (e.g., via the prevertebral ganglia) nervous systems. However, vertebrate studies show that when the vagus nerve is severed, the enteric nervous system continues to function.[7]
In vertebrates, the enteric nervous system includes efferent neurons, afferent neurons, and interneurons, all of which make the enteric nervous system capable of carrying reflexes and acting as an integrating center in the absence of CNS input. The sensory neurons report on mechanical and chemical conditions. Through intestinal muscles, the motor neurons control peristalsis and churning of intestinal contents. Other neurons control the secretion of enzymes. The enteric nervous system also makes use of more than 30 neurotransmitters, most of which are identical to the ones found in CNS, such as acetylcholine, dopamine, and serotonin. More than 90% of the body's serotonin lies in the gut, as well as about 50% of the body's dopamine, which is currently being studied to further our understanding of its utility in the brain.[18][19][20]
The enteric nervous system has the capacity to alter its response depending on such factors as bulk and nutrient composition.[21] In addition, the ENS contains support cells which are similar to astroglia of the brain and a diffusion barrier around the capillaries surrounding ganglia which is similar to the blood–brain barrier of cerebral blood vessels.[22]
Peristalsis
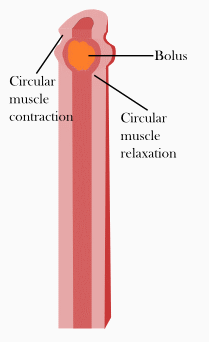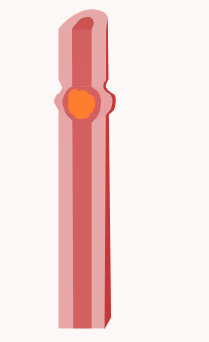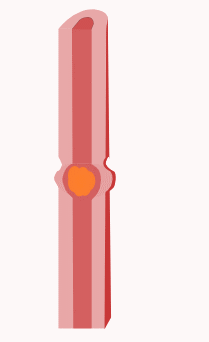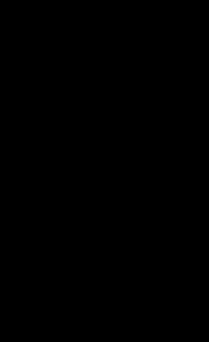
Peristalsis is a series of radially symmetrical contractions and relaxations of muscles which propagate down a muscular tube. In humans and other mammals, peristalsis is found in the smooth muscles of the digestive tract to propel contents through the digestive system. The word is derived from New Latin and comes from the Greek peristallein, "to wrap around," from peri-, "around" + stellein, "draw in, bring together; set in order". Peristalsis was discovered in 1899 by the work of physiologists William Bayliss and Ernest Starling. Working on the small intestines of dogs, they found that the response of increasing the pressure in the intestine caused the contraction of the muscle wall above the point of stimulation and the relaxation of the muscle wall below the point of stimulation.[23][6]
Segmentation
Segmentation contractions are the contractions in intestines carried out by the smooth muscle walls. Unlike peristalsis, which involves the contraction and relaxation of muscles in one direction, segmentation occurs simultaneously in both directions as the circular muscles alternatively contract. This allows for thorough mixing of intestinal contents, known as chyme, to allow greater absorption.
Secretion
The secretion of gastrointestinal hormones, such as gastrin and secretin, is regulated through cholinergic neurons residing in the walls of the digestive tract. Hormone secretion is controlled by the vagovagal reflex, where the neurons in the digestive tract communicate through both afferent and efferent pathways with the vagus nerve.[24]
المضامين الإكلينيكية
إن احتمال كون أمراض عصبية مثل الصَرَع، والشقيقة، والتوحد، قد تكون ناجمة عن اضطرابات الجهاز الهضمي ، يطرح بعض الأسئلة المحيرة فيما يتعلق بالممارسة الطبية الإكلينيكية والأبحاث الأكاديمية. وتتضمن هذه الأسئلة: ما هي طبيعة المرض؟ وهل يمكن قياسها؟ وإذا ظهر (أو افترض) وجود المرض؛ فما هي أفضل السبل العلاجية المتاحة؟ وهل هناك أي دليل يدعم المعالجات التي تركز على العوامل المرضية في الجهاز الهضمي؟… وأخيرا…هل يمكن شفاء هذه الأمراض؟ وللإجابة عن هذه الأسئلة؛ يدلنا التاريخ على أن العلاج الطبي للصَرَع والشقيقة في الماضي كثيرا ما كان يضم معالجات موجهة للملامح البطنية لهذه الأمراض. وبصورة خاصة، كان لأبحاث روبنسون تأثير كبير على بعض ممارسي "الطب البديل" – والذي كان لا يزال في مهده- في أواخر القرن التاسع عشر وأوائل القرن العشرين.
وعلى الرغم من أن المعالجة بتقويم العظام osteopathy قد أصبحت جزءا معروفا من الممارسة الطبية المعاصرة، إلا أن المبادئ والأساليب المعتمدة من قبل الممارسين التقليديين للمعالجة بتقويم العظام (مثل المعالجة اليدوية manipulative therapy، والحمية الغذائية، والمعالجة المائية hydrotherapy) قد استخدمت أيضا من قبل العديد من ممارسي بعض فروع الطب البديل، مثل تقويم العمود الفقري باليد chiropractic ، والمعالجة الطبيعية naturopathy. وقد تلقت هذه الأنماط العلاجية اهتماما متزايدا كمعالجات مكملة للطب التقليدي؛ فقد استخدمت المعالجة اليدوية في علاج الشقيقة والصَرَع، واستخدمت الحمية الغذائية في علاج الشقيقة. ويستخدم العلاج المولد للكيتونات ketogenic بصورة متزايدة في علاج الصَرَع، كما استخدمت المعالجة المائية وكمادات زيت الخروع على البطن في علاج الصَرَع والشقيقة.
ماذا بعد؟
يمكن تناول الأمراض العصبية ذات الملامح الجهازية (وخصوصا ذات الملامح الهضمية المهمة) من منظور الطب التكميلي، والذي يدرك دور الجهاز العصبي البطني من حيث السببيات والعلاج. وعن طريق التوفيق بين المقاربات التاريخية والإكلينيكية المبنية على أجهزة الجسم المختلفة، وبين الأبحاث الحديثة المتعلقة بالجهاز العصبي المعوي، يمكن خلق أسلوب تكميلي يجمع بين أفضل خصائص الممارسة الطبية الحديثة ، مع الأنظمة العلاجية التقليدية والبديلة، والمتوافقة مع الحقائق المؤكدة لعلمي التشريح والفيزيولوجيا (علم وظائف الأعضاء). وعلى الرغم من أن الصَرَع والشقيقة من بين الأمراض الشائعة، فإن النمط البطني لكل منهما نادر بصورة عامة. وبناء على المعطيات التاريخية والحديثة المتوافرة لدينا، يمكن القول بأن الصَرَع والشقيقة المجهولي المنشأ يمكن فهمهما بصورة أكبر إذا تم استقصاء الأعراض البطنية لكل منهما بصورة أكثر تفصيلا. وقد لا يكون الصَرَع والشقيقة البطنيان نادرين في الحقيقة، لكن الطب الحديث يعتبرهما نادري الحدوث لأن قليلا فقط من الاهتمام قد أعطي لفهم معنى الأعراض البطنية المرتبطة بهذه الحالات المرضية.
وربما كانت الأنماط المجهولة المنشأ لكلا المرضين تنطوي على أسباب بطنية. وبالمثل، فإن الجوانب البطنية لمرض التوحد تمثل علامات مميزة لمجموعة فرعية مهمة من هذا الاضطراب الذي يسبب كثيرا من الإعاقة للمصابين به والكثير من الضيق لذويهم. ويجب أن تركز الأبحاث المستقبلية المتعلقة بمسببات وعلاج هذه الحالات المرضية على اكتناف الجهاز العصبي المعوي فيها. ومن وجهة النظر الإكلينيكية، فقد يشير وجود ملامح بطنية مؤثرة إلى ضرورة أن تشتمل الخطة العلاجية على عناصر تقليدية (مثل الحمية، والمعالجة المائية للقولون العصبي، والمعالجة اليدوية)، والتي قد تؤثر بصورة إيجابية على الدماغ البطني والجهاز العصبي المعوي.
صور إضافية
انظر أيضاً
الهامش
- ^ أ ب Furness JB (15 April 2008). The Enteric Nervous System. John Wiley & Sons. pp. 35–38. ISBN 978-1-4051-7344-5.
- ^ Dorland's (2012). Dorland's Illustrated Medical Dictionary (32nd ed.). Elsevier Saunders. p. 1862. ISBN 978-1-4160-6257-8.
- ^ Pocock G, Richards C (2006). Human Physiology The Basis of Medicine (Third ed.). Oxford University Press. p. 63. ISBN 978-0-19-856878-0.
- ^ Barlow AJ, Wallace AS, Thapar N, Burns AJ (May 2008). "Critical numbers of neural crest cells are required in the pathways from the neural tube to the foregut to ensure complete enteric nervous system formation". Development. 135 (9): 1681–1691. doi:10.1242/dev.017418. PMID 18385256. S2CID 7401456.
- ^ Burns AJ, Thapar N (October 2006). "Advances in ontogeny of the enteric nervous system". Neurogastroenterology and Motility. 18 (10): 876–887. doi:10.1111/j.1365-2982.2006.00806.x. PMID 16961690. S2CID 34066966.
- ^ أ ب Gershon M (1998). The Second Brain. New York: HarperCollins. pp. 2–7. ISBN 0-06-018252-0.
- ^ أ ب Li Y, Owyang C (September 2003). "Musings on the wanderer: what's new in our understanding of vago-vagal reflexes? V. Remodeling of vagus and enteric neural circuitry after vagal injury". American Journal of Physiology. Gastrointestinal and Liver Physiology. 285 (3): G461–G469. doi:10.1152/ajpgi.00119.2003. PMID 12909562.
- ^ Pasricha PJ. "Stanford Hospital: Brain in the Gut - Your Health". YouTube.
- ^ Martinucci I, Blandizzi C, de Bortoli N, Bellini M, Antonioli L, Tuccori M, et al. (2015). "Genetics and pharmacogenetics of aminergic transmitter pathways in functional gastrointestinal disorders". Pharmacogenomics. 16 (5): 523–539. doi:10.2217/pgs.15.12. hdl:11577/3166305. PMID 25916523.
- ^ Smitka K, Papezova H, Vondra K, Hill M, Hainer V, Nedvidkova J (2013). "The role of "mixed" orexigenic and anorexigenic signals and autoantibodies reacting with appetite-regulating neuropeptides and peptides of the adipose tissue-gut-brain axis: relevance to food intake and nutritional status in patients with anorexia nervosa and bulimia nervosa". International Journal of Endocrinology. 2013 483145. doi:10.1155/2013/483145. PMC 3782835. PMID 24106499.
- ^ Young E. "Gut Instincts: The secrets of your second brain". New Scientist. Retrieved 8 April 2015.; alternate source at website: "NeuroScienceStuff". Archived from the original on 4 مايو 2013.
- ^ قالب:GrayPage
- ^ أ ب Hall JE (2011). "General Principles of Gastrointestinal Function". Guyton and Hal Textbook of Medical Physiology (12th ed.). Saunders Elsevier. p. 755. ISBN 978-1-4160-4574-8.
- ^ "The Enteric Nervous System". Retrieved 29 نوفمبر 2008.
- ^ Ross, Michael H, and Wojciech Pawlina. Histology: A Text and Atlas with Correlated Cell and Molecular Biology. Baltimore, MD: Lippincott Williams & Wilkins, 2006
- ^ "enteric nervous system" في قاموس دورلاند الطبي
- ^ Gershon & 1998 17.
- ^ Pasricha PJ. Brain in the Gut (video). Your Health. Stanford Hospital.
- ^ Martinucci I, Blandizzi C, de Bortoli N, Bellini M, Antonioli L, Tuccori M, et al. (2015). "Genetics and pharmacogenetics of aminergic transmitter pathways in functional gastrointestinal disorders". Pharmacogenomics. 16 (5): 523–539. doi:10.2217/pgs.15.12. hdl:11577/3166305. PMID 25916523.
- ^ Smitka K, Papezova H, Vondra K, Hill M, Hainer V, Nedvidkova J (2013). "The role of "mixed" orexigenic and anorexigenic signals and autoantibodies reacting with appetite-regulating neuropeptides and peptides of the adipose tissue-gut-brain axis: relevance to food intake and nutritional status in patients with anorexia nervosa and bulimia nervosa". International Journal of Endocrinology. 2013 483145. doi:10.1155/2013/483145. PMC 3782835. PMID 24106499.
- ^ Neunlist M, Schemann M (July 2014). "Nutrient-induced changes in the phenotype and function of the enteric nervous system". The Journal of Physiology. Wiley. 592 (14): 2959–2965. doi:10.1113/jphysiol.2014.272948. PMC 4214652. PMID 24907307. S2CID 37969390.
- ^ Silverthorn DU (2007). Human Physiology. San Francisco, CA: Pearson Education, Inc.
- ^ Keet AS. "The Pyloric Sphincteric Cylinder in health and disease". Retrieved 18 November 2013.
- ^ Herman MA, Cruz MT, Sahibzada N, Verbalis J, Gillis RA (January 2009). "GABA signaling in the nucleus tractus solitarius sets the level of activity in dorsal motor nucleus of the vagus cholinergic neurons in the vagovagal circuit". American Journal of Physiology. Gastrointestinal and Liver Physiology. 296 (1): G101–G111. doi:10.1152/ajpgi.90504.2008. PMC 2636929. PMID 19008339.