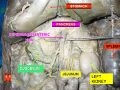
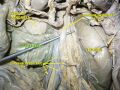
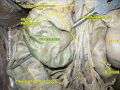
الاثنا عشر
| الاثنا عشر | |
|---|---|
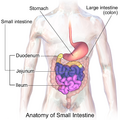
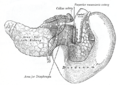
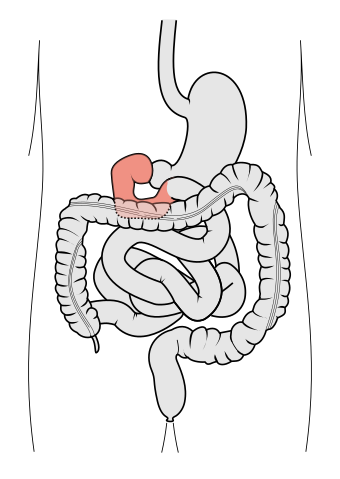 صورة للقناة الهضمية موضح عليها موقع الاثنا عشر. | |
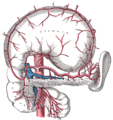
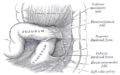
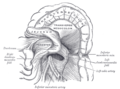
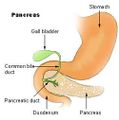
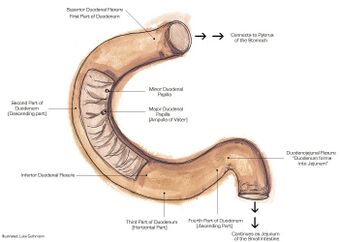 رسم تخطيطي للاثنا عشر البشري مع تسمية الأجزاء الرئيسية. | |
| Details | |
| النُطق | /ˌdjuːəˈdiːnəm/, US also /djuˈɒdɪnəm/[2] |
| السلف | المعي الأمامي (الجزء 1 و2)، المعي المتوسط (الجزء 3 و4) |
| جزء من | الأمعاء الدقيقة |
| الجهاز | الجهاز الهضمي |
| الشريان | الشريان الپنكرياسي الاثنى عشري السفلي، الشريان الپنكرياسي الاثنى عشري العلوي |
| الوريد | الأوردة الپنكرياسية الاثنى عشرية |
| العصب | العقد البطنية، المبهم[1] |
| المُعرفات | |
| اللاتينية | Duodenum |
| MeSH | D004386 |
| TA98 | A05.6.02.001 |
| TA2 | 2944 |
| FMA | 7206 |
| المصطلحات التشريحية | |
 |
| الأجزاء الرئيسية في |
| القناة الهضمية |
|---|
الاثنا عشر أو العَفَج (duodenum)، هو القسم الأول من الأمعاء الدقيقة[3] في معظم الفقاريات، بما في ذلك الثدييات، الزواحف، والطيور. في الثدييات، قد يكون الاثنا عشر هو الموقع الرئيسي لامتصاص الحديد.
يسبق الاثنا عشر الصائم واللفائفي وهو أقصر جزء من الأمعاء الدقيقة. في البشر، الاثنا عشر عبارة عن أنبوب مفصلي مجوف يبلغ طوله حوالي 25-38 سم، ويربط المعدة بالصائم، وهو الجزء الأوسط من الأمعاء الدقيقة.[4][5] يبدأ بالبصيلة الاثنا عشرية، وينتهي عند الثنية الاثنا عشرية الصائمية التي تميزها العضلة المعلقة.[6] يمكن تقسيم الاثنا عشر إلى أربعة أجزاء: الجزء الأول (العلوي)، والجزء الثاني (الهابط)، والجزء الثالث (المستعرض)، والجزء الرابع (الصاعد).[5]
نظرة عامة
الاثنا عشر هو القسم الأول من الأمعاء الدقيقة في معظم الفقاريات العليا، بما في ذلك الثدييات، الزواحف، والطيور. أما في الأسماك، فإن أقسام الأمعاء الدقيقة ليست واضحة تماماً، وقد يُستخدم مصطلحا المعي الأمامي أو المعي القريب بدلاً من الاثنا عشر.[7] قد يكون الاثنا عشر الموقع الرئيسي لامتصاص الحديد لدى الثدييات.[8]
في البشر، الاثنا عشر عبارة عن أنبوب مفصلي مجوف على شكل حرف C، يتراوح طوله بين 25 و38 سم، ويقع بجوار المعدة (ويربطها بالأمعاء الدقيقة). وهو مقسم تشريحياً إلى أربعة أقسام. يقع القسم الأول داخل الصفاق، بينما تقع أقسامه الأخرى خلف الصفاق.[9]
أجزاء الاثنا عشر
الجزء الأول أو العلوي من الاثنا عشر هو امتداد من البواب إلى مستوى ما بين البواب. وهو أعلى من باقي الأجزاء، عند مستوى الفقرة القطنية الأولى (L1). البصيلة الاثنا عشرية، التي يبلغ طولها حوالي 2 سم، هي الجزء الأول من الاثنا عشر وهي متوسعة قليلاً. البصيلة الاثنا عشرية هي بقايا المساريقا الاثنا عشرية، وهي مساريقا كانت تُعلق العضو من جدار البطن الخلفي في الحياة الجنينية.[10]
الجزء الأول من الاثنا عشر متحرك، ويتصل بالكبد بواسطة الرباط الكبدي الاثنا عشري للثرب الأصغر. وينتهي الجزء الأول من الاثنا عشر عند الزاوية، وهي الثنية الاثنا عشرية العلوية.[9]
أجزاء الاثنا عشر:
- الأمامي
- الخلفي
- العلوي
- السفلي
يبدأ الجزء الثاني أو النازل من الاثنا عشر عند الثنية الاثنا عشري العلوية. ويمتد الجزء سفلي إلى الحد السفلي للفقرة القطنية الثالثة (L3)، قبل أن ينعطف انعطافاً حاداً وسطياً إلى "الثنية الاثنا العشرية السفلية"، وهو نهاية الجزء النازل.[9]
تدخل القناة قناة الپنكرياسية والقناة الصفراوية المشتركة إلى الجزء النازل من الاثني عشر، عبر الحُليمة الاثنا عشرية الكبرى. ويحتوي الجزء الثاني من الاثنا عشر أيضاً على الحُليمة الاثنا عشرية الصغرى، وهي مدخل القناة الپنكرياسية الإضافية. ويقع ملتقى المعي الأمامي والمتوسط الجنيني أسفل الحُليمة الاثني عشرية الكبرى مباشرة.[9]
يبلغ طول الجزء الثالث، أو الأفقي، أو السفلي من الاثنا عشر حوالي 10-12 سم. يبدأ هذا الجزء من الثنية السفلية الاثنا عشرية ويمتد بشكل عرضي إلى اليسار، ماراً أمام الوريد الأجوف السفلي والأبهر البطني والعمود الفقري. يقع الشريان والوريد المساريقي العلوي أمام الجزء الثالث من الاثني عشر.[9] قد يتعرض هذا الجزء للضغط بين الأبهر والشريان المساريقي العلوي مما يسبب متلازمة الشريان المساريقي العلوي.
يمتد الجزء الرابع أو الصاعد من الاثنا عشر إلى الأعلى، ويتصل بالصائم عند الثنية الاثنا عشرية. يقع الجزء الرابع من الاثنا عشر عند مستوى الفقرة القطنية الثالثة (L3)، وقد يمر مباشرة فوق الشريان الأبهر أو قليلاً إلى يساره.[9]
إمدادات الدم
الجزء العلوي من الاثنا عشر، الذي يقعد بعد بواب المعدة مباشرة، لا يتغذى من الأقواس الشريانية. بل يتغذى من الشريان فوق الاثنا عشري والشريان الپنكرياسي الاثنا عشري الخلفي العلوي، بالإضافة إلى بعض فروع الشريان المعدي الثربي الأيمن والشريان الپنكرياسي الاثنا عشري الأمامي العلوي. وفي كثير من الأشخاص، يتغذى جزء من السنتيمتر الأول من الاثنا عشر أيضاً من فروع الشريان المعدي الأيمن.[11]
تُغذّى الأجزاء الثلاثة المتبقية (النازل، الأفقي، والصاعد) من الاثنا عشر بقوسين (حلقتين) من الشرايين، أحدهما (أمامي) أمام الاثني عشر والپنكرياس، والآخر خلفي (خلفهما). يتكون كل قوس من شريانين متفاغرين (متصلين). ينشأ الشريان العلوي لكل قوس من الشريان الپنكرياسي الاثنا عشري العلوي، الذي ينشأ بدوره من الشريان البطني عبر الشريان المعدي الاثنا عشري. أما الشريان السفلي لكل قوس فينشأ من الشريان الپنكرياسي الاثنا عشري السفلي، وهو فرع من الشريان المساريقي العلوي. يتكون القوس الأمامي من الشريان الپنكرياسي الاثنا عشري الأمامي العلوي والشريان الپنكرياسي الاثنا عشري الأمامي السفلي. يتكون القوس الخلفي من الشريان الپنكرياسي الاثنا عشري العلوي الخلفي والشريان الپنكرياسي الاثنا عشري السفلي الخلفي.[11][12]
تُغذي الأوعية الدموية القادمة من الأقواس الطبقة العضلية الخارجية قبل أن تُشكل ضفيرة (شبكة من الأوعية الدموية) في الطبقة تحت المخاطية (طبقة من النسيج الضام) تُسمى الضفيرة تحت المخاطية. وتستمر الأوعية من الضفيرة تحت المخاطية عبر الطبقة العضلية المخاطية (طبقة عضلية رقيقة أخرى) قبل أن تُشكل ضفيرة أخرى تحت النسيج الطلائي للزغابات المعوية، وهي الطبقة التي تُمتص فيها العناصر الغذائية. تُسمى هذه الأوعية التي تدخل الاثنا عشر من الأقواس أحياناً بالأوعية المستقيمة أو الشرايين المستقيمة.[11]
يتبع التصريف الوريدي للاثنا عشر مسار الشرايين بشكل رئيسي، ويصب في النهاية في الجهاز البوابي الكبدي. عادةً ما تكون الأقواس الوريدية سطحية بالنسبة للأقواس الشريانية. يصب الوريد الپنكرياسي الاثنا عشري الأمامي العلوي في الوريد الثربي المعدي الأيمن، وكذلك أوردة الجزء السفلي الأول من الاثنا عشر والبواب (الأوردة تحت البوابية). أما الجزء العلوي الأول من الاثنا عشر فيُصرف بواسطة الأوردة فوق البوابية، والتي قد تصب في الوريد البابي أو الوريد الپنكرياسي الاثنا عشري الخلفي العلوي، الذي يصب في الوريد البوابي. تصب الأوردة السفلية للأقواس في الوريد المساريقي العلوي، أو الوريد المساريقي السفلي، أو الوريد الطحالي، أو الوريد الصائمي الأول.[11]
من الناحية الجنينية، ينشأ الاثنا عشر من كل من المعي الأمامي والمتوسط، ويشكل الحد الفاصل بينهما. مع ذلك، تُعرَّف الأمعاء الوسطى جراحياً بأنها أجزاء الأمعاء التي يغذيها الشريان المساريقي العلوي. وبما أن الاثنا عشر يتغذى من كلٍّ من الشريان البطني والشريان المساريقي العلوي، فإن هذين التعريفين متشابهان لكنهما ليسا متطابقين تماماً.[11]
التصريف اللمفاوي
تتبع الأوعية اللمفاوية الشرايين في اتجاه عكسي. تصب الأوعية اللمفاوية الأمامية في العقد اللمفاوية الپنكرياسية الاثنا عشرية الواقعة على امتداد الشريانين الپنكرياسيين الاثنا عشريين العلوي والسفلي، ثم في العقد اللمفاوية البوابية (على امتداد الشريان المعدي الاثنا عشري). أما الأوعية اللمفاوية الخلفية فتمر خلف رأس الپنكرياس وتصب في العقد اللمفاوية المساريقية العلوية. وتتجه الأوعية اللمفاوية الصادرة من العقد اللمفاوية الاثنا عشرية في النهاية إلى العقد اللمفاوية البطنية.
علم الأنسجة
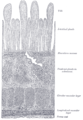
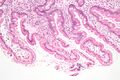
تحت المجهر، يحتوي الاثنا عشر على غشاء مخاطي زغابي. ويختلف هذا الغشاء عن الغشاء المخاطي للبواب، الذي يتصل مباشرة بالاثنا عشر. وكغيره من مكونات الجدار المعدي المعوي، يتكون الاثنا عشر من غشاء مخاطي، طبقة تحت مخاطية، طبقة عضلية خارجية، وغلالة خارجية. وتبطن الاثنا عشر غدد تُعرف بغدد برونر، تفرز المخاط والبيكربونات لمعادلة أحماض المعدة. وهذه غدد مميزة لا توجد في اللفائفي أو الصائم، وهما الجزءان الآخران من الأمعاء الدقيقة.[13]
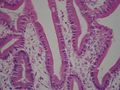
صورة مجهرية تُظهر داء الجيارديات في خزعة من الاثنا عشر (صبغة هـ. و أ.).
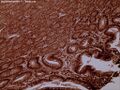
الاثنا عشر والحافة الفرشية (الزغابات الدقيقة).
الاختلافات
يُؤدي الارتباط التشريحي الوثيق بين الاثنا عشر والپنكرياس إلى اختلافات في الوظيفة بناءً على موقع واتجاه العضوين. يُسبب التشوه الخلقي المعروف بالپنكرياس الحلقي التفاف جزء من الپنكرياس حول الاثنا عشر. في حالة الپنكرياس الحلقي خارج الجدار، تُحيط القناة الپنكرياسية بالاثنا عشر، مما يُؤدي إلى انسداد معوي. أما في حالة الپنكرياس الحلقي داخل الجدار، فيتميز نسيج الپنكرياس باندماجه مع جدار الاثنا عشر، مما يُسبب تقرحات الاثنا عشر.[14]
This section requires expansion. (December 2013) |
التعبير الجيني والپروتيني
يُعبَّر عن حوالي 2000 جين مشفر للپروتين في الخلايا البشرية، ويُعبَّر عن 70% من هذه الجينات في الاثنا عشر الطبيعي.[15][16] يُعبَّر عن حوالي 300 من هذه الجينات بشكلٍ أكثر تحديداً في الاثنا عشر، بينما يُعبَّر عن عدد قليل جداً من الجينات حصرياً في الاثنا عشر. ويُعبَّر عن الپروتينات النوعية المقابلة في الغشاء المخاطي للاثنا عشر، ويُعبَّر عن العديد منها أيضاً في الأمعاء الدقيقة، مثل أمينوپپتيداز الألانين، وهو إنزيم هضمي، الإنزيم المحول للأنگيوتنسين، الذي يُشارك في تنظيم ضغط الدم، وپروتين RBP2، الذي يُشارك في امتصاص ڤيتامين أ.[17]
الوظيفة
يُعدّ الاثنا عشر مسؤولاً بشكل كبير عن هضم الطعام في الأمعاء الدقيقة، وذلك باستخدام الإنزيمات. كما يُنظّم الاثنا عشر معدل إفراغ المعدة عبر مسارات هرمونية. يُفرز سكرتين والكوليسيستوكنين من خلايا النسيج الطلائي للاثنا عشر استجابة للمحفزات الحمضية والدهنية الموجودة هناك عند فتح البواب، مما يؤدي إلى إفراز الكيموس المعدي إلى الاثنا عشر لمزيد من الهضم. يحفز ذلك الكبد والمرارة على إفراز العصارة الصفراوية، والپنكرياس على إفراز البيكربونات والإنزيمات الهاضمة مثل الترپسن، الليپاز، والأميلاز إلى الاثنا عشر حسب الحاجة.[18]
يُعد الاثنا عشر عضواً أساسياً في تنظيم تناول الطعام[19] والتحكم في نسبة سكر الدم.[20] يُعدّ الاثنا عشر، وهو الجزء الأول من الأمعاء الدقيقة، الموقع الأولي لامتصاص العناصر الغذائية في الجهاز الهضمي. يستشعر الاثنا عشر كمية العناصر الغذائية المتناولة وتكوينها، ويرسل إشارات إلى الكبد والپنكرياس والأنسجة الدهنية والمخ[21] من خلال الإطلاق المباشر وغير المباشر[22] للعديد من الهرمونات الرئيسية وجزيئات الإشارة، بما في ذلك پپتيدات الإنكرتين، پپتيد الأنسولين المعتمد على الگلوكوز (GIP) والپپتيد-1 مشابه للگلوكاگون (GLP-1)،[22] بالإضافة إلى الكوليسيستوكنين والسكرتين. كما يقوم الاثنا عشر بإرسال إشارات مباشرة إلى المخ عبر الألياف العصبية الواردة المبهمة مما يتيح التحكم العصبي في تناول الطعام ومستوى سكر الدم.[23] يحفز إفراز GIP وGLP-1 المعوي إفراز الأنسولين المعتمد على الگلوكوز من خلايا بيتا الپنكرياسية، وهو ما يُعرف بتأثير الإنكرتين.[24] تقوم پپتيدات الإنكرتين، وخاصة GLP-1 و GIP، بتنظيم إفراز هرمونات الجُزر، وتركيزات الگلوكوز، واستقلاب الدهون، وحركة الأمعاء، والشهية ووزن الجسم، ووظيفة مناعية.[25]
تتميز زغابات الاثنا عشر بمظهر يشبه الأوراق، وهو تركيب يمكن التعرف عليه نسيجياً. وتوجد غدد برونر، التي تفرز المخاط، حصراً في الاثنا عشر. ويتكون جدار الاثنا عشر من طبقة رقيقة جداً من الخلايا تُشكل الغشاء المخاطي العضلي.
الأهمية السريرية
التقرحات
تحدث قرح الاثنا عشر عادة بسبب عدوى بكتيريا الملوية البوابية. تعمل هذه البكتيريا، عبر آليات متعددة، على تآكل الغشاء المخاطي الواقي للاثنا عشر، مما يجعله أكثر عرضة للتلف بفعل أحماض المعدة. يُعد الجزء الأول من الاثنا عشر الموقع الأكثر شيوعاً للقرحة، حيث يلتقي الكيموس الحمضي بالغشاء المخاطي للاثنا عشر قبل أن يختلط بالإفرازات القلوية للاثنا عشر.[26] قد تسبب قرح الاثنا عشر ألماً متكرراً في البطن وعسر الهضم، وغالباً ما تُشخص باستخدام فحص الزفير باليوريا للكشف عن البكتيريا، والتنظير الداخلي لتأكيد وجود القرحة وأخذ خزعة. وفي حال علاجها، غالباً ما يتم ذلك باستخدام المضادات الحيوية التي تهدف إلى القضاء على البكتيريا، ومثبطات مضخة الپروتون ومضادات الحموضة لتقليل حموضة المعدة.[27]
الاضطراب الهضمي المناعي
تُحدد إرشادات الجمعية البريطانية لأمراض الجهاز الهضمي أن خزعة الاثنا عشر ضرورية لتشخيص المرض البطني لدى البالغين. ويُفضل إجراء الخزعة عندما يكون المريض يتبع حمية تحتوي على الگلوتين.[28]
السرطان
سرطان الاثنا عشر هو سرطان يصيب القسم الأول من الأمعاء الدقيقة. يُعد سرطان الاثنا عشر نادراً نسبياً مقارنةً بسرطان المعدة وسرطان القولون والمستقيم؛ إذ لا تشكل الأورام الخبيثة في الاثنا عشر سوى حوالي 0.3% من جميع أورام الجهاز الهضمي، لكنها تشكل حوالي نصف الأنسجة السرطانية التي تتطور في الأمعاء الدقيقة.[29] عند الفحص السيجي، غالباً ما يُلاحظ أنه سرطاناً غدياً، مما يعني أن النسيج السرطاني ينشأ من الخلايا الغدية في النسيج الطلائي المبطن للاثنا عشر.[30]
البدانة ومرض السكري
تؤدي الحمية الغربية إلى تضخم الغشاء المخاطي للاثنا عشر واختلال وظيفته، مما يؤدي إلى مقاومة الأنسولين ومرض سكري النمط الثاني والبدانة.[31][32] يتكون تضخم الغشاء المخاطي للاثنا عشر الناتج عن الحمية من زيادة في كتلة الغشاء المخاطي،[33] زيادة طول الزغابات،[31][34][35][36] انخفاض كثافة الخبايا،[31] انتشار الخلايا المعوية الصماء،[37] زيادة كتلة الخلايا المعوية،[38] وتراكم قطرات الدهون في الغشاء المخاطي.[39][40] تشمل الاختلالات الوظيفية في الاثنا عشر الناتجة عن الحمية زيادة امتصاص العناصر الغذائية في الاثنا عشر،[34][41][42][43] تغير إفراز الهرمونات في الاثنا عشر،[31][37] وتغير وظيفة الخلايا العصبية الواردة المبهمة المعوية.[44]
الالتهاب
يُطلق على التهاب الذي يُصيب الاثنا عشر اسم التهاب الاثنا عشر (duodenitis). وهناك عدة أسباب معروفة لحدوثه.[45] يُعد الداء البطني والتهاب الأمعاء من الأسباب المعروفة.[46]
أبحاث
علاج محتمل لسكري النمط الثاني
 مقالة مفصلة: إعادة تسطيح الغشاء المخاطي للاثنا عشر
مقالة مفصلة: إعادة تسطيح الغشاء المخاطي للاثنا عشر
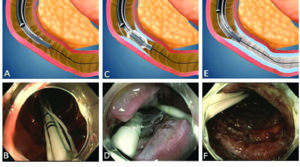
أصبح الاثنا عشر هدفاً للعلاج الأيضي بفضل النتائج التي أظهرها في جراحات البدانة آمنة، والملاحظة الدقيقة بأن تجاوز الاثنا عشر أو استبعاده أو تغيير تعرضه للمغذيات يُحدث تغييرات أيضية إيجابية. يُعد إعادة تسطيح الغشاء المخاطي للاثنا عشر (DMR) إجراءً تنظيرياً حديثاً أثبت فعاليته في تحسين التحكم في مستوى سكر الدم لدى مرضى سكري النمط الثاني، بغض النظر عن تغيرات مؤشر كتلة الجسم. يتضمن هذا الإجراء رفع الغشاء المخاطي بشكل دائري باستخدام قسطرة، يليه استئصال الغشاء المخاطي للاثنا عشر حرارياً-مائياً، وعادة ما يخرج المريض في نفس اليوم.
التجارب العلمية
بحسب دراسة دولية أجرتها عدة مراكز بحثية عام 2020، نشرها المركز الوطني لمعلومات التقانة الحيوية بالولايات المتحدة، خضع مرضى سكري النمط الثاني (مؤشر كتلة الجسم 24-40) الذين يتناولون أدوية خافضة لسكر الدم عن طريق الفم بجرعات ثابتة، لعملية تعديل جرعة الدواء. تم الحفاظ على استقرار جرعة أدوية خفض سكر الدم لمدة 24 أسبوعاً على الأقل بعد العملية. خلال فترة المتابعة، تم تحديد وتحليل مستويات الهموگلوبين الگلايكوزيلاتي (HbA1c)، وسكر الدم الصائم، والوزن، وإنزيمات الكبد، ومؤشر مقاومة الأنسولين (HOMA-IR)، والآثار الجانبية، ورضا المرضى عن العلاج، باستخدام تحليل التباين للقياسات المتكررة مع تصحيح بونفروني.[47]
شملت الدراسة 46 حالة، خضع 37 منهم (80%) لعملية استئصال كامل للغشاء المخاطي للاثنا عشر، وتحليل بيانات 36 منهم في النهاية؛ أما الحالات المتبقية، فقد لوحظت لديهم مشاكل تقنية في الغالب. عانت 24 حالة من عرض جانبي واحد على الأقل (52%) مرتبط بعملية استئصال الغشاء المخاطي للاثنا عشر. من بين هذه الأعراض، كانت 81% منها خفيفة. أُبلغ عن عرض جانبي خطير واحد فقط، ولم يُبلغ عن أي أعراض جانبية غير متوقعة. بعد 24 أسبوعاً (3 أشهر) من عملية استئصال الغشاء المخاطي للاثنا عشر (ن=36)، تحسنت مستويات الهموگلوبين الگلايكوزيلاتي (HbA1c) بمقدار 10±2 مليمول/مول (0.9%±0.2%)، p<0.001، وسكر الدم الصائم (FPG) بمقدار 1.7±0.5 مليمول/لتر، p<0.001)، ومؤشر مقاومة الأنسولين (HOMA-IR) بمقدار 2.9±1.1، p<0.001، وانخفض الوزن بشكل طفيف بمقدار 2.5±0.6 كجم، p<0.001، وانخفضت مستويات ناقلات أمين الكبد. استمرت هذه التأثيرات الإيجابية لمدة 12 شهراً. لم يرتبط التغير في مستوى الهموگلوبين الگلايكوزيلاتي (HbA1c) بانخفاض طفيف في الوزن. وقد تحسنت درجات الرضا عن علاج مرض السكري بشكل ملحوظ. خلُصت الدراسة إلى أن استئصال الغشاء المخاطي للاثنا عشر عن طريق المنظار هو إجراء طبي عملي وآمن، وقد حقق تحسناً مستداماً في مستويات سكر الدم لدى مرضى سكري النمط الثاني، الذين لا يتحكمون بمستويات السكر لديهم بشكلٍ مثاليي، والذين يتناولون أدوية خافضة للسكر عن طريق الفم، بغض النظر عن فقدان الوزن.
التقنية
يتضمن إجراء إعادة تسطيح الغشاء المخاطي للاثنا عشر إدخال كاميرا مرنة (منظار داخلي) عبر الفم، ثم تمريرها عبر المعدة إلى الاثنا عشر في الأمعاء الدقيقة. تُجرى العملية بواسطة أطباء الجهاز الهضمي، حيث يقوم الطبيب بإدخال المنظار المثبت في نهايته بالونات مُسخنة، ويُؤدي هذا العلاج الحراري إلى تعديل بطانة خلايا الاثنا عشر. هذه الخلايا مسؤولة عن امتصاص الگلوكوز واستجابة الجسم الهرمونية للتحكم في مستوى سكر الدم. يهدف هذا الإجراء إلى تغيير السطح الداخلي للاثنا عشر بشكل آمن وفعال، ما يُغيّر طريقة معالجة الجسم للسكريات من النظام الغذائي. من شأن هذه العملية أن تُحسّن بدورها مستوى سكر الدم، وهو أمر بالغ الأهمية لمرضى سكري النمط الثاني. وعادة ما يخرج المريض في نفس اليوم.[48]
الآثار الجانبية
يعتبر إجراء إعادة تسطيح الغشاء المخاطي للاثنا عشر آمناً بشكل عام ويتحمله الجسم جيداً، حيث تكون معظم الآثار الجانبية المبلغ عنها خفيفة وقصيرة الأمد. تشمل الأعراض الجانبية الشائعة والبسيطة أعراضاً هضمية مثل ألم البطن، الغثيان، الإسهال، التهاب الحلق، أو الشعور بالتوعك. قد تشمل المضاعفات النادرة والخطيرة تضيق الاثنا عشر أو، في حالات نادرة جداً، حدوث ثقب.
التكلفة
تبلغ تكلفة إجراء إعادة تسطيح الغشاء المخاطي للاثنا عشر في الولايات المتحدة حوالي 40.000 دولار. في ألمانيا، جعلت المستشفيات العامة والشراكات الصحية العالمية هذا الإجراء مجانياً لغير المواطنين كجزء من برامج تجريبية دولية. يحصل المريض على تكلفة الانتقال (السفر من خارج ألمانيا، أو من داخلها) وكذلك تكلفة الإجراء والخدمات التي تقدمها المستشفى.[49]
انظر أيضاً
- الپنكرياس
- مفاغرة قناة الصفراء بالإثنا عشر - إجراء جراحي لإنشاء اتصال بين القناة الصفراوية المشتركة وجزء بديل من الاثنا عشر.
معرض الصور
المصادر
- ^ Nosek, Thomas M. "Section 6/6ch2/s6ch2_30". Essentials of Human Physiology. Archived from the original on 2016-03-24.
- ^ Jones, Daniel (2011), Cambridge English Pronouncing Dictionary (18 ed.), Cambridge University Press, ISBN 978-0-521-15255-6
- ^ "NCI Dictionary of Cancer Terms". National Cancer Institute. Retrieved 2022-06-07.
The first part of the small intestine. It connects to the stomach. The duodenum helps to further digest food coming from the stomach. It absorbs nutrients (vitamins, minerals, carbohydrates, fats, proteins) and water from food so they can be used by the body.
- ^ "Duodenum: MedlinePlus Medical Encyclopedia". MedlinePlus. Retrieved 2022-06-07.
It is located between the stomach and the middle part of the small intestine. After foods mix with stomach acid, they move into the duodenum, where they mix with bile from the gallbladder and digestive juices from the pancreas.
- ^ أ ب Nolan, D. J. (2002). "Radiology of the Duodenum". Radiological Imaging of the Small Intestine. Medical Radiology. Berlin, Heidelberg: Springer Berlin Heidelberg. pp. 247–259. doi:10.1007/978-3-642-56231-0_6. ISBN 978-3-642-62993-8. ISSN 0942-5373.
duodenum is a C-shaped hollow organ forming an incomplete circle around the head of the pancreas. ...it is normally examined as part of the upper gastrointestinal tract.
- ^ van Gijn J; Gijselhart JP (2011). "Treitz and his ligament". Ned. Tijdschr. Geneeskd. 155 (8): A2879. PMID 21557825.
- ^ Guillaume, Jean; Praxis Publishing; Sadasivam Kaushik; Pierre Bergot; Robert Metailler (2001). Nutrition and Feeding of Fish and Crustaceans. Springer. p. 31. ISBN 978-1-85233-241-9. Retrieved 2009-01-09.
- ^ Latunde-Dada GO; Van der Westhuizen J; Vulpe CD; et al. (2002). "Molecular and functional roles of duodenal cytochrome B (Dcytb) in iron metabolism". Blood Cells Mol. Dis. 29 (3): 356–60. doi:10.1006/bcmd.2002.0574. PMID 12547225.
- ^ أ ب ت ث ج ح Drake, Richard L.; Vogl, Wayne; Tibbitts, Adam W.M. Mitchell; illustrations by Richard; Richardson, Paul (2005). Gray's anatomy for students. Philadelphia: Elsevier/Churchill Livingstone. ISBN 978-0-8089-2306-0.
- ^ Singh, Inderbir; GP Pal (2012). "13". Human Embryology (9 ed.). Delhi: Macmillan Publishers India. p. 163. ISBN 978-93-5059-122-2.
- ^ أ ب ت ث ج Androulakis, John; Colborn, Gene L.; Skandalakis, Panagiotis N.; Skandalakis, Lee J.; Skandalakis, John E. (2000-02-01). "Embryologic and Anatomic Basis of Duodenal Surgery". Surgical Clinics of North America. 80 (1): 171–199. doi:10.1016/S0039-6109(05)70401-1. ISSN 0039-6109.
- ^ Aasen, S.; Lundin, K. E. A. (2013), Hamm, Bernd; Ros, Pablo R., eds. (in en), Stomach Duodenum Normal Anatomy, Function and Congenital Anomalies, Berlin, Heidelberg: Springer, pp. 367–382, doi:, ISBN 978-3-642-13327-5, https://link.springer.com/referenceworkentry/10.1007/978-3-642-13327-5_17, retrieved on 2025-03-09
- ^ Deakin, Barbara Young; et al. (2006). Wheater's functional histology: a text and colour atlas (5th ed.). [Edinburgh?]: Churchill Livingstone/Elsevier. ISBN 978-0-443-06850-8.
- ^ Borghei, Peyman; Sokhandon, Farnoosh; Shirkhoda, Ali; Morgan, Desiree E. (January 2013). "Anomalies, Anatomic Variants, and Sources of Diagnostic Pitfalls in Pancreatic Imaging". Radiology (in الإنجليزية). 266 (1): 28–36. doi:10.1148/radiol.12112469. ISSN 0033-8419. PMID 23264525.
- ^ "The human proteome in duodenum - The Human Protein Atlas". www.proteinatlas.org. Retrieved 2017-09-26.
- ^ Uhlén, Mathias; Fagerberg, Linn; Hallström, Björn M.; Lindskog, Cecilia; Oksvold, Per; Mardinoglu, Adil; Sivertsson, Åsa; Kampf, Caroline; Sjöstedt, Evelina (2015-01-23). "Tissue-based map of the human proteome". Science (in الإنجليزية). 347 (6220) 1260419. doi:10.1126/science.1260419. ISSN 0036-8075. PMID 25613900. S2CID 802377.
- ^ Gremel, Gabriela; Wanders, Alkwin; Cedernaes, Jonathan; Fagerberg, Linn; Hallström, Björn; Edlund, Karolina; Sjöstedt, Evelina; Uhlén, Mathias; Pontén, Fredrik (2015-01-01). "The human gastrointestinal tract-specific transcriptome and proteome as defined by RNA sequencing and antibody-based profiling". Journal of Gastroenterology (in الإنجليزية). 50 (1): 46–57. doi:10.1007/s00535-014-0958-7. ISSN 0944-1174. PMID 24789573. S2CID 21302849.
- ^ Chandra, Rashmi; Liddle, Rodger A. (September 2014). "Recent advances in the regulation of pancreatic secretion". Current Opinion in Gastroenterology (in الإنجليزية الأمريكية). 30 (5): 490–494. doi:10.1097/MOG.0000000000000099. ISSN 0267-1379. PMC 4229368. PMID 25003603.
- ^ Woodward, Orla R. M.; Gribble, Fiona M.; Reimann, Frank; Lewis, Jo E. (2022). "Gut peptide regulation of food intake – evidence for the modulation of hedonic feeding". The Journal of Physiology (in الإنجليزية). 600 (5): 1053–1078. doi:10.1113/JP280581. ISSN 1469-7793. PMID 34152020.
- ^ Drucker, Daniel J. (2006-03-01). "The biology of incretin hormones". Cell Metabolism (in English). 3 (3): 153–165. doi:10.1016/j.cmet.2006.01.004. ISSN 1550-4131. PMID 16517403.
{{cite journal}}: CS1 maint: unrecognized language (link) - ^ Bany Bakar, Rula; Reimann, Frank; Gribble, Fiona M. (December 2023). "The intestine as an endocrine organ and the role of gut hormones in metabolic regulation". Nature Reviews Gastroenterology & Hepatology (in الإنجليزية). 20 (12): 784–796. doi:10.1038/s41575-023-00830-y. ISSN 1759-5053. PMID 37626258.
- ^ أ ب Hansen, Lene; Holst, Jens J (2002-12-31). "The effects of duodenal peptides on glucagon-like peptide-1 secretion from the ileum: A duodeno–ileal loop?". Regulatory Peptides. 110 (1): 39–45. doi:10.1016/S0167-0115(02)00157-X. ISSN 0167-0115. PMID 12468108.
- ^ Thorens, Bernard; Larsen, Philip Just (July 2004). "Gut-derived signaling molecules and vagal afferents in the control of glucose and energy homeostasis". Current Opinion in Clinical Nutrition & Metabolic Care (in الإنجليزية الأمريكية). 7 (4): 471–478. doi:10.1097/01.mco.0000134368.91900.84. ISSN 1363-1950. PMID 15192452.
- ^ Nauck, Michael A.; Meier, Juris J. (February 2018). "Incretin hormones: Their role in health and disease". Diabetes, Obesity and Metabolism. 20 (S1): 5–21. doi:10.1111/dom.13129. ISSN 1462-8902. PMID 29364588.
- ^ Campbell, Jonathan E.; Drucker, Daniel J. (2013-06-04). "Pharmacology, physiology, and mechanisms of incretin hormone action". Cell Metabolism. 17 (6): 819–837. doi:10.1016/j.cmet.2013.04.008. ISSN 1932-7420. PMID 23684623.
- ^ Smith, Margaret E. The Digestive System.
- ^ Colledge, Nicki R.; Walker, Brian R.; Ralston, Stuart H., eds. (2010). Davidson's principles and practice of medicine (21st ed.). Edinburgh: Churchill Livingstone/Elsevier. pp. 871–874. ISBN 978-0-7020-3085-7.
- ^ Ludvigsson, J. F.; Bai, J. C.; Biagi, F.; Card, T. R.; Ciacci, C.; Ciclitira, P. J.; Green, P. H. R.; Hadjivassiliou, M.; Holdoway, A.; van Heel, D. A.; Kaukinen, K.; Leffler, D. A.; Leonard, J. N.; Lundin, K. E. A.; McGough, N.; Davidson, M.; Murray, J. A.; Swift, G. L.; Walker, M. M.; Zingone, F.; Sanders, D. S. (2014). "Diagnosis and management of adult coeliac disease: Guidelines from the British Society of Gastroenterology". Gut. 63 (8): 1210–1228. doi:10.1136/gutjnl-2013-306578. ISSN 0017-5749. PMC 4112432. PMID 24917550.
- ^ Fagniez, Pierre-Louis; Rotman, Nelly (2001). Malignant tumors of the duodenum. Zuckschwerdt.
- ^ "Definition of adenocarcinoma - NCI Dictionary of Cancer Terms". National Cancer Institute. Retrieved 12 July 2024.
- ^ أ ب ت ث Aliluev, Alexandra; Tritschler, Sophie; Sterr, Michael; Oppenländer, Lena; Hinterdobler, Julia; Greisle, Tobias; Irmler, Martin; Beckers, Johannes; Sun, Na; Walch, Axel; Stemmer, Kerstin; Kindt, Alida; Krumsiek, Jan; Tschöp, Matthias H.; Luecken, Malte D. (2021-09-22). "Diet-induced alteration of intestinal stem cell function underlies obesity and prediabetes in mice". Nature Metabolism (in الإنجليزية). 3 (9): 1202–1216. doi:10.1038/s42255-021-00458-9. ISSN 2522-5812. PMC 8458097. PMID 34552271.
- ^ Clara, Rosmarie; Schumacher, Manuel; Ramachandran, Deepti; Fedele, Shahana; Krieger, Jean-Philippe; Langhans, Wolfgang; Mansouri, Abdelhak (January 2017). "Metabolic Adaptation of the Small Intestine to Short- and Medium-Term High-Fat Diet Exposure: INTESTINAL METABOLIC ADAPTATION TO HFD". Journal of Cellular Physiology (in الإنجليزية). 232 (1): 167–175. doi:10.1002/jcp.25402. PMID 27061934.
- ^ Hvid, Henning; Jensen, Stina Rikke; Witgen, Brent M.; Fledelius, Christian; Damgaard, Jesper; Pyke, Charles; Rasmussen, Thomas Bovbjerg (2016). "Diabetic Phenotype in the Small Intestine of Zucker Diabetic Fatty Rats". Digestion (in الإنجليزية). 94 (4): 199–214. doi:10.1159/000453107. ISSN 0012-2823. PMID 27931035.
- ^ أ ب Taylor, Samuel R.; Ramsamooj, Shakti; Liang, Roger J.; Katti, Alyna; Pozovskiy, Rita; Vasan, Neil; Hwang, Seo-Kyoung; Nahiyaan, Navid; Francoeur, Nancy J.; Schatoff, Emma M.; Johnson, Jared L.; Shah, Manish A.; Dannenberg, Andrew J.; Sebra, Robert P.; Dow, Lukas E. (2021-09-09). "Dietary fructose improves intestinal cell survival and nutrient absorption". Nature (in الإنجليزية). 597 (7875): 263–267. doi:10.1038/s41586-021-03827-2. ISSN 0028-0836. PMC 8686685. PMID 34408323.
- ^ Dailey, Megan J. (September 2014). "Nutrient-induced intestinal adaption and its effect in obesity". Physiology & Behavior (in الإنجليزية). 136: 74–78. doi:10.1016/j.physbeh.2014.03.026. PMC 4182169. PMID 24704111.
- ^ Sagher, F. A.; Dodge, J. A.; Johnston, C. F.; Shaw, C.; Buchanan, K. D.; Carr, K. E. (1991). "Rat small intestinal morphology and tissue regulatory peptides: effects of high dietary fat". British Journal of Nutrition (in الإنجليزية). 65 (1): 21–28. doi:10.1079/BJN19910062. ISSN 0007-1145. PMID 1705145.
- ^ أ ب Gniuli, D.; Calcagno, A.; Dalla Libera, L.; Calvani, R.; Leccesi, L.; Caristo, M. E.; Vettor, R.; Castagneto, M.; Ghirlanda, G.; Mingrone, G. (October 2010). "High-fat feeding stimulates endocrine, glucose-dependent insulinotropic polypeptide (GIP)-expressing cell hyperplasia in the duodenum of Wistar rats". Diabetologia (in الإنجليزية). 53 (10): 2233–2240. doi:10.1007/s00125-010-1830-9. ISSN 0012-186X. PMID 20585935.
- ^ Verdam, Froukje J.; Greve, Jan Willem M.; Roosta, Sedigheh; van Eijk, Hans; Bouvy, Nicole; Buurman, Wim A.; Rensen, Sander S. (2011-02-01). "Small Intestinal Alterations in Severely Obese Hyperglycemic Subjects". The Journal of Clinical Endocrinology & Metabolism (in الإنجليزية). 96 (2): E379–E383. doi:10.1210/jc.2010-1333. ISSN 0021-972X. PMID 21084402.
- ^ Sferra, Roberta; Pompili, Simona; Cappariello, Alfredo; Gaudio, Eugenio; Latella, Giovanni; Vetuschi, Antonella (2021-07-06). "Prolonged Chronic Consumption of a High Fat with Sucrose Diet Alters the Morphology of the Small Intestine". International Journal of Molecular Sciences (in الإنجليزية). 22 (14): 7280. doi:10.3390/ijms22147280. ISSN 1422-0067. PMC 8303301. PMID 34298894.
- ^ D'Aquila, Theresa; Zembroski, Alyssa S.; Buhman, Kimberly K. (2019-03-05). "Diet Induced Obesity Alters Intestinal Cytoplasmic Lipid Droplet Morphology and Proteome in the Postprandial Response to Dietary Fat". Frontiers in Physiology. 10: 180. doi:10.3389/fphys.2019.00180. ISSN 1664-042X. PMC 6413465. PMID 30890954.
- ^ Dyer, J.; Wood, I. S.; Palejwala, A.; Ellis, A.; Shirazi-Beechey, S. P. (2002-02-01). "Expression of monosaccharide transporters in intestine of diabetic humans". American Journal of Physiology. Gastrointestinal and Liver Physiology (in الإنجليزية). 282 (2): G241–G248. doi:10.1152/ajpgi.00310.2001. ISSN 0193-1857.
- ^ Fiorentino, Teresa Vanessa; Suraci, Evelina; Arcidiacono, Gaetano Paride; Cimellaro, Antonio; Mignogna, Chiara; Presta, Ivan; Andreozzi, Francesco; Hribal, Marta Letizia; Perticone, Francesco; Donato, Giuseppe; Luzza, Francesco; Sesti, Giorgio (2017-11-01). "Duodenal Sodium/Glucose Cotransporter 1 Expression Under Fasting Conditions Is Associated With Postload Hyperglycemia". The Journal of Clinical Endocrinology & Metabolism (in الإنجليزية). 102 (11): 3979–3989. doi:10.1210/jc.2017-00348. ISSN 0021-972X.
- ^ Fiorentino, Teresa Vanessa; De Vito, Francesca; Suraci, Evelina; Marasco, Raffaella; Hribal, Marta Letizia; Luzza, Francesco; Sesti, Giorgio (March 2023). "Obesity and overweight are linked to increased sodium-glucose cotransporter 1 and glucose transporter 5 levels in duodenum". Obesity (in الإنجليزية). 31 (3): 724–731. doi:10.1002/oby.23653. ISSN 1930-7381.
- ^ de Lartigue, Guillaume; Barbier de la Serre, Claire; Espero, Elvis; Lee, Jennifer; Raybould, Helen E. (2012-03-07). Gaetani, Silvana (ed.). "Leptin Resistance in Vagal Afferent Neurons Inhibits Cholecystokinin Signaling and Satiation in Diet Induced Obese Rats". PLOS ONE (in الإنجليزية). 7 (3) e32967. doi:10.1371/journal.pone.0032967. ISSN 1932-6203. PMC 3296757. PMID 22412960.
- ^ Serra S, Jani PA (2006). "An approach to duodenal biopsies". J. Clin. Pathol. 59 (11): 1133–50. doi:10.1136/jcp.2005.031260. PMC 1860495. PMID 16679353.
- ^ Alper, Arik; Hardee, Steven; Rojas-velasquez, Danilo; Escalera, Sandra; Morotti, Raffaella A; Pashankar, Dinesh S. (February 2016). "Prevalence, clinical, endoscopic and pathological features of duodenitis in children". Journal of Pediatric Gastroenterology and Nutrition. 62 (2): 314–316. doi:10.1097/MPG.0000000000000942. ISSN 0277-2116. PMC 4724230. PMID 26252915.
- ^ "Endoscopic duodenal mucosal resurfacing for the treatment of type 2 diabetes mellitus: one year results from the first international, open-label, prospective, multicentre study". المركز الوطني لمعلومات التقانة الحيوية. 2019-06-22. Retrieved 2026-02-04.
- ^ "What is Duodenal mucosal resurfacing (DMR)?". drrehanhaidry.com. Retrieved 2026-02-05.
- ^ "In a groundbreaking development, Germany is now offering what's being called a permanent cure for Type 2 diabetes". argosaki. 2026-02-04. Retrieved 2026-02-04.
وصلات خارجية
هذا المقال يستخدم مصطلحات التشريح؛ لنظرة عامة، انظر مصطلحات التشريح.