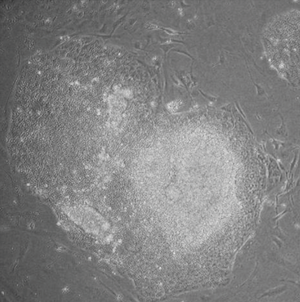
خلية جذعية محرضة متعددة القدرات
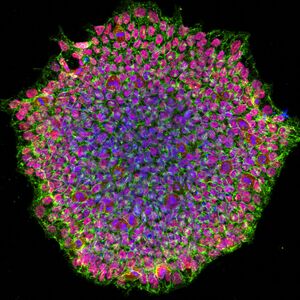
الخلايا الجذعية المحرضة متعددة القدرات أو الخلايا الجذعية المستحثة عديدة القدرات (Induced pluripotent stem cells، تُعرف أيضاً بخلايا iPS أو iPSCs)، هي نوع من الخلايا الجذعية متعددة القدرات التي يمكن توليدها مباشرة من خلية جسدية. وقد طوّر تقنية الخلايا الجذعية المحرضة متعددة القدرات كل من شنيا ياماناكا وكازوتوشي تاكاهاشي في كيوتو باليابان، حيث أظهرا معاً عام 2006 أن إدخال أربعة جينات محددة (تُسمى c-Myc، Oct4، Sox2 وKLF4)، والمعروفة مجتمعة باسم عوامل ياماناكا، والتي تُشفّر عوامل النسخ، يمكن أن يحوّل الخلايا الجسدية إلى خلايا جذعية متعددة القدرات.[1] حصل شنيا ياماناكا على جائزة نوبل للطب 2012 إلى جانب السير جون گوردون، "لاكتشاف أن الخلايا البالغة يمكن إعادة برمجتها لتصبح متعددة القدرات".[2]
تُبشر الخلايا الجذعية متعددة القدرات بآفاق واعدة في مجال الطب التجديدي.[3] لأنها تستطيع التكاثر إلى أجل غير مسمى، فضلاً عن كونها قادرة على إنتاج جميع أنواع الخلايا الأخرى في الجسم (مثل الخلايا العصبية، خلايا القلب، خلايا الپنكرياس، وخلايا الكبد)، فإنها تمثل مصدراً وحيداً للخلايا التي يمكن استخدامها لاستبدال تلك المفقودة بسبب التلف أو المرض.
أشهر أنواع الخلايا الجذعية متعددة القدرات هي الخلايا الجذعية الجنينية. ومع ذلك، بما أن توليد الخلايا الجذعية الجنينية ينطوي على تدمير (أو على الأقل تلاعب)[4] في مرحلة ما قبل انغراس الجنين، أثير جدل واسع حول استخدام الخلايا الجذعية. ويمكن الآن الحصول على خطوط خلايا جذعية جنينية متطابقة مع المريض باستخدام تقنية نقل نواة الخلية الجسدية (SCNT).[citation needed]
بما أن الخلايا الجذعية المحرضة متعددة القدرات يمكن استخلاصها مباشرة من أنسجة البالغين، فإنها لا تغني عن الحاجة إلى الأجنة فحسب، بل يمكن إنتاجها بطريقة تراعي خصائص المريض، مما يعني أن كل فرد يمكن أن يمتلك خط خلايا جذعية متعددة القدرات خاص به. ويمكن استخدام هذه الإمدادات غير المحدودة من الخلايا ذاتية الانغراس لإجراء عمليات زرع دون خطر الرفض المناعي. ورغم أن تقنية الخلايا الجذعية المحرضة متعددة القدرات لم تصل بعد إلى مرحلة تُعتبر فيها عمليات الزرع العلاجية آمنة، إلا أن هذه الخلايا تُستخدم على نطاق واسع في جهود اكتشاف الأدوية الشخصية وفهم أساس المرض الخاص بكل مريض.[5]
أطلق ياماناكا على الخلايا الجذعية المحرضة متعددة القدرات اختصار (iPSCs) حيث حرف "i" الصغير نظراً لشعبية جهاز الآيپود ومنتجات شركة آپل الأخرى.[6][7][8][9]
في ندوة نوبل الخاصة به، أشار ياماناكا إلى العمل الرائد السابق لهارولد وينتروب حول دور پروتين تحديد الخلايا العضلية 1 (MyoD) في إعادة برمجة مصير الخلية إلى سلالة عضلية باعتباره مقدمة هامة لاكتشاف الخلايا الجذعية المحرضة متعددة القدرات.[10]
الإنتاج
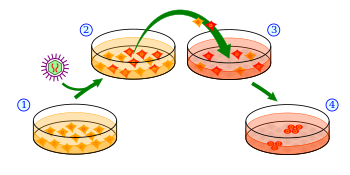
تُستخلص الخلايا الجذعية المحرضة متعددة القدرات عادة عن طريق إدخال نواتج مجموعات محددة من الجينات المرتبطة بتعدد القدرات، أو ما يُعرف "بعوامل إعادة البرمجة"، إلى نوع خلوي معين. تتكون المجموعة الأصلية من عوامل إعادة البرمجة (المعروفة أيضاً بعوامل ياماناكا) من عوامل النسخ Oct4 (Pou5f1)، Sox2، Klf4، وcMyc. على الرغم من أن هذا المزيج هو الأكثر شيوعاً في إنتاج الخلايا الجذعية المحرضة متعددة القدرات، إلا أنه يمكن استبدال كل عامل من هذه العوامل وظيفياً بعوامل نسخ ذات صلة، أو ميكرو رنا (microRNA)، أو جزيئات صغيرة، أو حتى جينات غير ذات صلة مثل محددات السلالة.[11] من الواضح أيضاً أن العوامل المحفزة للانقسام الخلوي مثل C-MYC/L-MYC أو تثبيط نقاط التفتيش في دورة الخلية، مثل p53، هي قنوات لخلق حالة خلوية متوافقة لإعادة برمجة الخلايا الجذعية المحرضة متعددة القدرات.[12]
يُعدّ استخلاص الخلايا الجذعية المحرضة متعددة القدرات عملية بطيئة وغير فعّالة في العادة، إذ تستغرق من أسبوع إلى أسبوعين لخلايا الجرذان، ومن ثلاثة إلى أربعة أسابيع للخلايا البشرية، بكفاءة تتراوح بين 0.01% و0.1%. مع ذلك، فقد أُحرز تقدم ملحوظ في تحسين كفاءة هذه العملية وتقليل الوقت اللازم للحصول على الخلايا الجذعية المحرضة متعددة القدرات. عند إدخال عوامل إعادة البرمجة، تبدأ الخلايا بتكوين مستعمرات تُشبه الخلايا الجذعية متعددة القدرات، والتي يُمكن عزلها بناء على شكلها، أو الظروف التي تُحفّز نموّها، أو من خلال التعبير عن الواسمات السطحية أو الجينات المرشد.
الجيل الأول (الجرذان)
أُنتجت الخلايا الجذعية المحرضة متعددة القدرات لأول مرة بواسطة شنيا ياماناكا وكازوتوشي تاكاهاشي في جامعة كيوتو اليابانية، عام 2006.[1] افترض الباحثون أن الجينات الهامة لوظيفة الخلايا الجذعية الجنينية قد تكون قادرة على تحريض حالة جنينية في الخلايا البالغة. اختاروا أربعة وعشرين جيناً سبق تحديدها كجينات هامة في الخلايا الجذعية الجنينية، واستخدموا الڤيروسات القهقرية لنقل هذه الجينات إلى أرومات ليفية للجرذان. تم تعديل الأرومات الليفية وراثياً بحيث يمكن عزل أي خلايا تعيد تنشيط الجين الخاص بالخلايا الجذعية الجنينية، Fbx15، باستخدام المضادات الحيوية.
بعد إضافة جميع العوامل الأربعة والعشرين، ظهرت مستعمرات شبيهة بالخلايا الجذعية الجنينية، أعادت تنشيط الجين المخبر Fbx15، وتمكنت من التكاثر بلا حدود. ولتحديد الجينات اللازمة لإعادة البرمجة، أزال الباحثون عاملاً واحداً في كل مرة من مجموعة العوامل الأربعة والعشرين. وبهذه العملية، حددوا أربعة عوامل، هي Oct4 وSox2 وcMyc وKlf4، كان كل منها ضرورياً، ومجتمعةً كافيةً لتوليد مستعمرات شبيهة بالخلايا الجذعية الجنينية تحت ضغط إعادة تنشيط الجين Fbx15.
الجيل الثاني (الجرذان)
في يونيو 2007، قامت ثلاث مجموعات بحثية منفصلة، من بينها مجموعة ياماناكا، ومجموعة تعاونية بين جامعتي هارڤرد وكاليفورنيا-لوس أنجلس، ومعهد مساتشوستس للتكنولوجيا، بنشر دراسات حسنت بشكلٍ كبيرٍ من أسلوب إعادة البرمجة، مما أدى إلى ظهور خلايا جذعية محرضة متعددة القدرات لا يمكن تمييزها عن الخلايا الجذعية الجنينية. وعلى عكس الجيل الأول من الخلايا الجذعية المحرضة متعددة القدرات، أنتجت خلايا جذعية محرضة متعددة القدرات من الجيل الثاني لجرذان هجينة قابلة للحياة، وساهمت في تكوين السلالة الجرثومية للجرذان، وبذلك حققت "المعيار الذهبي" للخلايا الجذعية متعددة القدرات.
اشتقت هذه الخلايا الجذعية المحرضة متعددة القدرات من الجيل الثاني من أرومات ليفية لجرذان عن طريق التعبير بوساطة الڤيروسات القهقرية عن عوامل النسخ الأربعة نفسها (Oct4، Sox2، cMyc، Klf4). مع ذلك، وبدلاً من استخدام Fbx15 لاختيار الخلايا متعددة القدرات، استخدم الباحثون الجين نانونگ، وهو جين ذو أهمية وظيفية في الخلايا الجذعية الجنينية. وباستخدام هذه الاستراتيجية المختلفة، تمكن الباحثون من إنتاج خلايا جذعية محرضة متعددة القدرات مطابقة وظيفياً للخلايا الجذعية الجنينية.[13][14][15][16]
الخلايا الجذعية المحرضة متعددة القدرات البشرية
التوليد من الخلايا الليفية البشرية
في نوفمبر 2007 أُعلن عن إعادة برمجة الخلايا البشرية إلى خلايا جذعية محرضة متعددة القدرات، من قبل مجموعتين بحثيتين مستقلتين: شنيا ياماناكا من جامعة كيوتو باليابان، رائد تقنية الخلايا الجذعية المحرضة متعددة القدرات الأصلية، وجيمس طومسون من جامعة وسكنسن-ماديسون، الذي كان أول من استخلص الخلايا الجذعية الجنينية البشرية. وباستخدام المبدأ نفسه المُستخدم في إعادة برمجة الجرذان، نجحت مجموعة ياماناكا في تحويل الخلايا الليفية البشرية إلى خلايا جذعية محرضة متعددة القدرات باستخدام الجينات المحورية الأربعة نفسها، وهي Oct4 وSox2 وKlf4 وcMyc، وذلك باستخدام نظام ڤيروسي قهقري،[17] بينما استخدم طومسون وزملاؤه مجموعة مختلفة من العوامل، وهي Oct4 وSox2 وNanog وLin28، باستخدام نظام ڤيروسي بطيئ.[18]
التوليد من أنواع خلايا إضافية
يتطلب الحصول على الأرومات الليفية لإنتاج الخلايا الجذعية المحرضة متعددة القدرات أخذ خزعة من الجلد، وقد كان هناك توجه نحو تحديد أنواع الخلايا التي يسهل الوصول إليها.[19][20] عام 2008، أُشتقت الخلايا الجذعية المحرضة متعددة القدرات من الخلايا الكيراتينية البشرية، والتي يمكن الحصول عليها من شعرة واحدة.[21][22] عام 2010، أُشتقت الخلايا الجذعية المحرضة متعددة القدرات من خلايا الدم المحيطية،[23][24] وفي عام 2012، تم إنتاج الخلايا الجذعية المحرضة متعددة القدرات من الخلايا الطلائية الكلوية الموجودة في البول.[25]
وتشمل الاعتبارات الأخرى لنوع الخلية الأولية الحمل الطفري (على سبيل المثال، قد تحمل خلايا الجلد المزيد من الطفرات بسبب التعرض للأشعة فوق البنفسجية)،[19][20] الوقت اللازم لتوسيع نطاق الخلايا الأولية،[19] والقدرة على التمايز إلى نوع معين من الخلايا.[26]
الجينات المستخدمة للإنتاج
يعتمد توليد الخلايا الجذعية المحرضة بشكل حاسم على عوامل النسخ المستخدمة في عملية التحريض.
تم تحديد الجين Oct-3/4 وبعض جينات عائلة SOX (Sox1، Sox2، Sox3، وSox15) كمنظمات نسخية أساسية تشارك في عملية التحفيز، ويؤدي غيابها إلى استحالة التحريض. ومع ذلك، تم تحديد جينات إضافية، بما في ذلك بعض أفراد عائلة عوامل Klf (Klf1، Klf2، Klf4، وKlf5)، وعائلة Myc (c-myc، L-myc، وN-myc)، وجين نانونگ، وLIN28، لزيادة كفاءة التحريض.[citation needed]
- يُعدّ Oct-3/4 (Pou5f1) أحد أفراد عائلة عوامل النسخ الثمانية (Oct)، ويلعب دوراً حاسماً في الحفاظ على القدرة على التمايز إلى أنواع متعددة من الخلايا. يؤدي غياب Oct-3/4 في الخلايا التي تحتوي على Oct-3/4+، مثل الخلايا الجينية الأولية والخلايا الجذعية الجنينية، إلى تمايز تلقائي للخلايا المغذية، وبالتالي فإن وجود Oct-3/4 يُكسب الخلايا الجذعية الجنينية القدرة على التمايز إلى أنواع متعددة من الخلايا. تفشل جينات أخرى عديدة في عائلة Oct، بما في ذلك الجينات القريبة من Oct-3/4، مثل Oct1 وOct6، في تحريض التعبير الجيني، مما يُثبت حصرية Oct-3/4 في عملية التحريض. أظهر شولر أن الإفراط في التعبير عن Oct4 أثناء إعادة البرمجة يسبب تغييرات فوق جينية تؤدي إلى تدهور جودة الخلايا الجذعية المحرضة متعددة القدرات. بالمقارنة مع OSKM (Oct4، Sox2، Klf4 و c-Myc)، فإن إعادة برمجة SKM (Sox2، Klf4 و c-Myc) الجديدة تولد خلايا جذعية محرضة متعددة القدرات ذات إمكانات نمو مكافئة للخلايا الجذعية الجنينية، كما تم تحديده من خلال قدرتها على توليد كامل للخلايا الجذعية المحرضة متعددة القدرات للجرذان من خلال تكميل الجنين الرباعي الصبغي.[27][28] يمكن أيضاً توليد خلايا جذعية محرضة متعددة القدرات ذات إمكانات نمو أعلى عن طريق تعزيز التماثل بين Oct4 وSox2 باستخدام عامل Sox هجين.[29]
- عائلة Sox: ترتبط عائلة عوامل النسخ Sox بالحفاظ على القدرة على التمايز إلى أنواع متعددة من الخلايا على غرار Oct-3/4، على الرغم من أنها مرتبطة بالخلايا الجذعية متعددة القدرات والخلايا الجذعية أحادية القدرة على عكس Oct-3/4، الذي يتم التعبير عنه حصرياً في الخلايا الجذعية متعددة القدرات. في حين أن Sox2 كان الجين الأولي المستخدم للتحريض بواسطة ياماناكا وزملاءه، جاينيش وزملاؤه، وطومسون وزملاؤه، فقد عُثر على عوامل نسخ أخرى في عائلة Sox تعمل بشكل جيد في عملية التحريض. يُنتج جين Sox1 خلايا جذعية محرضة متعددة القدرات بكفاءة مماثلة لجين Sox2، كما تُنتج جينات Sox3 وSox15 وSox18 خلايا جذعية محرضة متعددة القدرات، وإن كانت بكفاءة أقل. وقد قام ڤليتشكو وزملاؤه بهندسة عامل إعادة برمجة فائق مُهجن، يُسمى Sox2-17 أو "سوپر-سوكس"، والذي عزز أو سمح بإنتاج خلايا جذعية محرضة متعددة القدرات من الجرذان والبشر وقرود المكاك والخنازير والأبقار.[29]
- عائلة Klf:تم تحديد Klf4 من عائلة عوامل النسخ Klf في البداية بواسطة ياماناكا وزملاءه. وتم تأكيده بواسطة جاينيش وزملاؤه. كعامل لتوليد خلايا جذعية محرضة متعددة القدرات من الجرذان، وقد أثبت ياماناكا وزملاءه أنه عامل لتوليد الخلايا الجذعية المحرضة متعددة القدرات البشرية. مع ذلك، أفاد طومسون وزملاؤه أن Klf4 غير ضروري لتوليد الخلايا الجذعية المحرضة متعددة القدرات البشرية، بل إنه فشل في توليدها. ووجد أن Klf2 وKlf4 عوامل قادرة على توليد هذه الخلايا، وكذلك الجينات ذات الصلة Klf1 وKlf5، وإن كان ذلك بكفاءة أقل.
- عائلة Myc: تُعدّ عائلة عوامل النسخ Myc من الجينات المسرطنة الأولية التي لها دور في تكون السرطان. وقد أثبت كل من ياماناكا وزملاؤه وجاينيش وزملاؤه أن c-myc عاملٌ مُشارك في توليد الخلايا الجذعية المحرضة متعددة القدرات في الجرذان، كما أثبت ياماناكا وزملاؤه أنه عامل مشارك في توليد الخلايا الجذعية المحرضة متعددة القدرات البشرية. مع ذلك، فإن استخدام عائلة جينات "myc" في تحفيز الخلايا الجذعية المحرضة متعددة القدرات، كما في دراسات طومسون وزملاؤه وياماناكا وزملاؤه، يُثير مخاوف بشأن إمكانية استخدام هذه الخلايا كعلاجات سريرية، إذ أصيب 25% من الجرذان التي زُرعت بخلايا جذعية محرضة متعددة القدرات مُحفزة بواسطة c-myc بأورام مسخية قاتلة. وقد تم تحديد N-myc وL-myc كبديلين للجين c-myc، وبكفاءة مماثلة.
- نانونگ (Nanog): في الخلايا الجذعية الجنينية، يُعدّ جين نانونگ، إلى جانب Oct-3/4 وSox2، ضرورياً لتعزيز القدرة على التمايز إلى أنواع متعددة من الخلايا. ولذلك، كان من المفاجئ أن يُشير ياماناكا وزملاؤه إلى أن نانونگ غير ضروري للتحريض، على الرغم من أن طومسون وزملاؤه قد أفادوا بإمكانية توليد خلايا جذعية محرضة متعددة الخلايا باستخدام نانونگ كأحد العوامل.
- LIN28: LIN28 هو پروتين مرتبط بالميكرو رنا[30] يُعبَّر عنه في الخلايا الجذعية الجنينية وخلايا سرطان الأجنة المرتبطة بالتمايز والتكاثر. وقد أثبت طومسون وزملاؤه أن LIN28 هو أحد عوامل توليد الخلايا الجذعية المحرضة متعددة القدرات بالاشتراك مع OCT4 وSOX2 ونانونگ.[18]
- Glis1: Glis1 هو عامل نسخ يمكن استخدامه مع Oct-3/4 وSox2 وKlf4 لتحريض القدرة على التمايز إلى أنواع متعددة من الخلايا. ويُوفر العديد من المزايا عند استخدامه بدلاً من C-myc.[31]
تحديات إعادة برمجة الخلايا إلى حالة تعددية القدرات
على الرغم من أن الأساليب التي ابتكرها ياماناكا وزملاؤه أثبتت إمكانية إعادة برمجة الخلايا البالغة إلى خلايا جذعية محرضة متعددة القدرات، إلا أن هناك تحديات لا تزال مرتبطة بهذه التقنية:
- انخفاض الكفاءة: بشكل عام، كانت عملية تحويل الخلايا الجذعية المحرضة متعددة القدرات منخفضة للغاية. على سبيل المثال، بلغت نسبة إعادة برمجة الخلايا الجسدية إلى خلايا جذعية محرضة متعددة القدرات في دراسة ياماناكا الأصلية على الجرذان 0.01-0.1%.[1] قد يعكس انخفاض معدل الكفاءة الحاجة إلى توقيت دقيق، وتوازن، ومستويات تعبير مطلقة لجينات إعادة البرمجة. وقد يشير أيضاً إلى الحاجة إلى تغييرات جينية أو فوق جينية نادرة في مجموعة الخلايا الجسدية الأصلية أو في الاستزراع المطول. ومع ذلك، تم مؤخراً اكتشاف مسار لإعادة البرمجة بكفاءة يتطلب خفض تنظيم مُركب إعادة تشكيل وإزالة أسيتيل الجسيم النووي (NuRD). يؤدي الإفراط في التعبير عن Mbd3، وهي وحدة فرعية من NuRD، إلى تثبيط تحفيز الخلايا الجذعية المحرضة متعددة القدرات. من ناحية أخرى، يؤدي استنفاد Mbd3 إلى تحسين كفاءة إعادة البرمجة،[32] ينتج عن ذلك إعادة برمجة الخلايا الجذعية المحرضة متعددة القدرات بشكل حتمي ومتزامن (كفاءة تقارب 100% في غضون سبعة أيام من خلايا الجرذان والخلايا البشرية).[33]
- الإدخال الجينومي: إن التكامل الجينومي لعوامل النسخ يحد من فائدة نهج عامل النسخ بسبب خطر إدخال الطفرات في جينوم الخلية المستهدفة.[34] تتمثل إحدى الاستراتيجيات الشائعة لتجنب إدخال الجينوم في استخدام ناقل مختلف للإدخال. وقد تم استكشاف الپلازميدات، الڤيروسات الغدانية ونواقل الجين الناقل، لكن غالباً ما يكون لهذا الأمر ثمن يتمثل في انخفاض الإنتاجية.[35][36][37]
- القدرة على إحداث الأورام: اعتماداً على الطرق المستخدمة، قد تشكل إعادة برمجة الخلايا البالغة للحصول على الخلايا الجذعية المحرضة متعددة القدرات مخاطر كبيرة تحد من استخدامها في البشر. على سبيل المثال، إذا استُخدمت الڤيروسات لتعديل جينوم الخلايا، فقد يتم تحريض التعبير عن الجينات المسرطنة. في فبراير 2008، أعلن العلماء عن اكتشاف تقنية قادرة على إزالة الجينات المسرطنة بعد تحفيز القدرة على التمايز إلى أنواع مختلفة من الخلايا، مما يزيد من إمكانية استخدام الخلايا الجذعية المحرضة متعددة القدرات في علاج الأمراض البشرية.[38] في دراسة أخرى، أفاد ياماناكا بإمكانية إنتاج الخلايا الجذعية المحرضة متعددة القدرات دون وجود الجين الورمي c-Myc. استغرقت العملية وقتاً أطول ولم تكن بنفس الكفاءة، لكن الكائنات الهجينة الناتجة لم تُصب بالسرطان.[39] يؤدي تعطيل أو حذف مثبط الورم p53، وهو منظم رئيسي للسرطان، إلى زيادة كفاءة إعادة البرمجة بشكل كبير.[40] لذا، يبدو أن هناك مفاضلة بين كفاءة إعادة البرمجة وتكون الأورام.
- إعادة البرمجة غير المكتملة: تواجه عملية إعادة البرمجة تحدياً يتمثل في اكتمالها. ويُعدّ هذا تحدياً خاصاً نظراً لضرورة إعادة صياغة الشفرة فوق الجينية على مستوى الجينوم لتتوافق مع نوع الخلية المستهدفة، وذلك لإعادة برمجة الخلية بشكل كامل. مع ذلك، تمكنت ثلاث مجموعات بحثية منفصلة من إيجاد خلايا جذعية محرضة متعددة القدرات مشتقة من الأرومة الليفية الجنينية للجرذان (MEF)، والتي يمكن حقنها في الكيسات الأرومية رباعية الصيغة الصبغية، مما أدى إلى ولادة جرذان حية مشتقة بالكامل من خلايا جذعية محرضة متعددة القدرات، وبالتالي حسم الجدل الدائر حول تكافؤ الخلايا الجذعية الجنينية والخلايا الجذعية المحرضة متعددة القدرات فيما يتعلق بقدرتها على التمايز إلى أنواع مختلفة من الخلايا.[41]
يلخص الجدول الموجود على اليمين الاستراتيجيات والتقنيات الرئيسية المستخدمة لتطوير الخلايا الجذعية المحرضة متعددة القدرات في السنوات الخمس الأولى بعد الإنجاز الذي حققه ياماناكا وزملاؤه عام 2006. وتمثل الصفوف ذات الألوان المتشابهة الدراسات التي استخدمت استراتيجيات مماثلة لإعادة البرمجة.
المنهجيات البديلة
محاكاة عوامل النسخ بالمواد الكيميائية
تتمثل إحدى الاستراتيجيات الرئيسية لتجنب المشكلتين (1) و(2) في استخدام جزيئات صغيرة تحاكي تأثيرات عوامل النسخ. تعوض هذه المركبات عن عامل إعادة البرمجة الذي لا يستهدف الجينوم بفعالية أو يفشل في إعادة البرمجة لسبب آخر، مما يزيد من كفاءة إعادة البرمجة. كما أنها تتجنب مشكلة التكامل الجينومي، التي تُسهم في بعض الحالات في تكون الأورام. أُجريت دراسات رئيسية باستخدام هذه الاستراتيجية عام 2008. درس ميلتون وزملاؤه تأثيرات حمض الفالبرويك، وهو مثبط لإنزيم histone deacetylase (HDAC). ووجدوا أنه يزيد من كفاءة إعادة البرمجة بمقدار 100 ضعف (مقارنةً بطريقة ياماناكا التقليدية لعامل النسخ).[42] اقترح الباحثون أن هذا المركب يحاكي الإشارات التي يُحدثها عادة عامل النسخ c-Myc. كما اقترحوا آلية تعويض مماثلة لمحاكاة تأثيرات Sox2. عام 2008، استخدم دينگ وزملاؤه تثبيط إنزيم ناقل ميثيل الهيستون (HMT) باستخدام BIX-01294 بالتزامن مع تنشيط قنوات الكالسيوم في غشاء الپلازما لزيادة كفاءة إعادة البرمجة.[43] أفاد دينگ وزملاؤه من جامعة بكين في يوليو 2013 بإمكانية إنتاج خلايا جذعية محرضة متعددة القدرات دون أي تعديل جيني. استخدموا مزيجاً من سبعة مركبات جزيئية صغيرة، من بينها DZNep، لتحريض الخلايا الجسدية للجرذان على التحول إلى خلايا جذعية أطلقوا عليها اسم خلايا CiPS، بكفاءة بلغت 0.2%، وهي نسبة مماثلة لتلك التي تُحقق باستخدام تقنيات إنتاج الخلايا الجذعية المحرضة متعددة القدرات التقليدية. أُدخلت خلايا CiPS إلى أجنة جرذان نامية، ووُجد أنها تُساهم في تكوين جميع أنواع الخلايا الرئيسية، مما يُثبت قدرتها المتعددة.[44][45]
استعرض دينگ وزملاؤه بديلاً لإعادة برمجة عوامل النسخ باستخدام مواد كيميائية شبيهة بالأدوية. من خلال دراسة عملية التحول الطلائي-اللحمي الوسيطي (mesenchymal-epithelial transition) (MET)، التي تُحفز فيها الخلايا الليفية على التحول إلى حالة شبيهة بالخلايا الجذعية، حدد فريق دينگ مادتين كيميائيتين - مثبط ALK5، SB431412، ومثبط MEK (كيناز الپروتين المنشط بالميتوجين)، PD0325901 - وُجد أنهما يزيدان من كفاءة الطريقة الجينية التقليدية بمقدار 100 ضعف. وبإضافة مركب ثالث معروف بدوره في مسار بقاء الخلية، وهو الثيازوڤيڤين، زادت الكفاءة بمقدار 200 ضعف. كما أدى استخدام مزيج هذه المركبات الثلاثة إلى تقليص مدة عملية إعادة برمجة الأرومات الليفية البشرية من أربعة أسابيع إلى أسبوعين.[46][47]
في أبريل 2009، أُثبتت إمكانية توليد الخلايا الجذعية المحرضة متعددة القدرات دون أي تعديل جيني للخلايا البالغة: إذ يكفي معالجة الخلايا بشكل متكرر بپروتينات معينة تُوجه إلى الخلايا عبر مثبتات متعددة الأرجينين لتحفيز تعدد القدرات.[48] الاختصار المستخدم للإشارة إلى تلك الخلايا الجذعية المحرضة متعددة القدرات هو piPSCs (الخلايا الجذعية متعددة القدرات المحرضة بالپروتين).
النواقل البديلة
تتمثل إحدى الاستراتيجيات الرئيسية الأخرى لتجنب مشكلات مثل تكون الأورام وانخفاض الإنتاجية في استخدام أشكال بديلة من النواقل: الپيروسات الغدية، الپلازميدات، ومركبات الدنا أو الپروتين العارية.
عام 2008، استخدم هوشدلينگر وزملاؤه ڤيروساً غدياً لنقل عوامل النسخ الأربعة اللازمة إلى الدنا لخلايا الجلد والكبد لدى الجرذان، مما أدى إلى خلايا مطابقة للخلايا الجذعية الجنينية. تتميز الڤيروسات الغدية عن النواقل الأخرى، كالڤيروسات والڤيروسات القهقرية، بأنه لا تًدخل أياً من جيناتها الخاصة في الخلية المضيفة المستهدفة، وبالتالي تتجنب احتمالية حدوث طفرات إدخالية.[43] عام 2009، أثبت فريد وزملاؤه نجاح إعادة برمجة الأرومات الليفية البشرية إلى خلايا جذعية محرضة متعددة القدرات.[49] ومن المزايا الأخرى لاستخدام الڤيروسات الغدية أنها تحتاج فقط إلى التواجد لفترة وجيزة من الوقت حتى تعاد البرمجة الفعالة.
وفي عام 2008 أيضاً، وجد ياماناكا وزملاؤه أنه بإمكانهم نقل الجينات الأربعة الضرورية باستخدام پلازميد.[35] نجح فريق ياماناكا في إعادة برمجة خلايا الجرذان عن طريق نقل جينين پلازميديين يحملان عوامل إعادة البرمجة؛ عبّر الپلازميد الأول عن الجين c-Myc، بينما عبّر الثاني عن العوامل الثلاثة الأخرى (Oct4، Klf4، وSox2). ورغم أن طرق الپلازميد تتجنب الڤيروسات، إلا أنها لا تزال تتطلب جينات محفزة للسرطان لإتمام عملية إعادة البرمجة. أما المشكلة الرئيسية الأخرى في هذه الطرق فهي أنها أقل كفاءة بكثير مقارنةً بطرق الڤيروسات القهقرية. علاوة على ذلك، فقد ثبت أن الپلازميدات المنقولة تندمج في جينوم الخلية المضيفة، وبالتالي لا تزال تشكل خطر الطفرات الإدخالية. ونظراً لأن الطرق غير الڤيروسية أظهرت مستويات كفاءة منخفضة للغاية، فقد حاول الباحثون إنقاذ هذه التقنية بفعالية باستخدام ما يُعرف بنظام PiggyBac Transposon. وقد أثبتت العديد من الدراسات أن هذا النظام قادر على توصيل عوامل إعادة البرمجة الرئيسية بكفاءة دون ترك أي طفرات في جينوم الخلية المضيفة. يعتمد PiggyBac Transposon System على إعادة استئصال الجينات الخارجية، مما يقضي على مشكلة الطفرات الإدخالية.[citation needed]
اكتساب تعددية القدرات بواسطة المحرض
في يناير 2014، نُشرت مقالتان تزعمان أنه يمكن توليد نوع من الخلايا الجذعية متعددة القدرات عن طريق تعريض الخلايا لأنواع معينة من الإجهاد (السموم البكتيرية، أو درجة حموضة منخفضة تبلغ 5.7، أو الضغط الفيزيائي)؛ وقد أطلق على الخلايا الناتجة اسم خلايا STAP، اختصاراً تعددية القدرات بواسطة المحرض (stimulus-triggered acquisition of pluripotency).[50]
في ضوء الصعوبات التي واجهتها معامل أخرى في تكرار نتائج الدراسة المفاجئة، دعا أحد المؤلفين المشاركين في مارس 2014 إلى سحب المقالات.[51] في 4 يونيو 2014، وافقت المؤلفة الرئيسية، أوبوكاتا، على سحب كلتا الورقتين البحثيتين[52] بعد أن تبين أنها ارتكبت "سوء سلوك بحثي" بحسب ما خلص إليه تحقيق أجرته ريكن في 1 أبريل 2014.[53]
جزيئات الرنا
تُعدّ جزيئات الميكرو رنا (MicroRNA) جزيئات قصيرة من الرنا ترتبط بتسلسلات مكملة على مرسال الرنا (mRNA)]] وتمنع التعبير عن الجين. ويمكن استخدام قياس الاختلافات في التعبير عن الرنا في الخلايا الجذعية المحرضة متعددة القدرات للتنبؤ بقدرتها على التمايز.[54] يمكن أيضاً استخدام إضافة الميكرو رنا لتعزيز إمكانات الخلايا الجذعية المحرضة متعددة القدرات. وقد أُقترح العديد من الآليات.[54] تعمل جزيئات الميكرو رنا الخاصة بالخلايا الجذعية الجنينية (مثل miR-291 و miR-294 و miR-295) على تعزيز كفاءة التعددية المحرضة من خلال العمل في اتجاه مجرى c-Myc.[55] يمكن للميكرو رنا أيضاً أن تمنع التعبير عن مثبطات عوامل النسخ الأربعة لياماناكا، وقد تكون هناك آليات إضافية تحريض إعادة البرمجة حتى في غياب عوامل النسخ الخارجية المضافة.[54]
الهوية
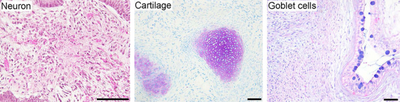
تتشابه الخلايا الجذعية المحرضة متعددة القدرات مع الخلايا الجذعية الطبيعية متعددة القدرات، مثل الخلايا الجذعية الجنينية، في جوانب عديدة، مثل التعبير عن جينات وپروتينات معينة للخلايا الجذعية، أنماط مثيلة الدنا، وقت التضاعف، تكون الأجسام الجنينية، تكون الأورام المسخية، تكون الكيميرا القابلة للحياة، القدرة والتمايز، لكن لا يزال مدى علاقتها بالخلايا الجذعية الطبيعية متعددة القدرات قيد التقييم.[1]
وُجد أن التعبير الجيني ومستويات H3K4me3 وH3K27me3 على مستوى الجينوم متشابهة للغاية بين الخلايا الجذعية الجنينية والخلايا الجذعية المحرضة متعددة القدرات.[56][citation needed] كانت الخلايا الجذعية المحرضة متعددة القدرات المولدة مشابهة بشكل ملحوظ للخلايا الجذعية متعددة القدرات المعزولة طبيعياً (مثل الخلايا الجذعية الجنينية للجرذان (mESCs) وللبشر (hESCs)) في الجوانب التالية، مما يؤكد هوية الخلايا الجذعية المحرضة متعددة القدرات وأصالتها وقدرتها على التمايز إلى أنواع مختلفة من الخلايا مقارنة بالخلايا الجذعية متعددة القدرات المعزولة طبيعياً:
- الخصائص الحيوية الخلوية
- المورفولوجيا: كانت الخلايا الجذعية المحرضة متعددة القدرات متشابهة مورفولوجياً مع الخلايا الجذعية الجنينية. تميزت كل خلية بشكلها الدائري، ونوية كبيرة، وسيتوپلازم قليل. كما كانت مستعمرات الخلايا الجذعية المحرضة متعددة القدرات مشابهة لمستعمرات الخلايا الجذعية الجنينية. شكلت الخلايا الجذعية المحرضة متعددة القدرات البشرية مستعمرات حادة الحواف، مسطحة، ومتراصة بإحكام، تشبه مستعمرات الخلايا الجذعية الجنينية البشرية، بينما شكلت الخلايا الجذعية المحرضة متعددة القدرات للجرذان مستعمرات مشابهة لمستعمرات الخلايا الجذعية الجنينية للجرذان، أقل تسطحاً وأكثر تكتلاً من مستعمرات الخلايا الجذعية الجنينية البشرية.
- خصائص النمو: يُعد كل من زمن التضاعف والنشاط الانقسامي الفتيلي من الركائز الأساسية للخلايا الجذعية الجنينية، إذ يجب أن تتجدد الخلايا الجذعية ذاتياً كجزء من تعريفها. وقد أظهرت الخلايا الجذعية المحرضة متعددة القدرات نشاطاً انقسامياً، وتجدداً ذاتياً فعالاً، وتكاثراً، وانقساماً بمعدل يُعادل معدل الخلايا الجذعية الجنينية.
- مؤشرات الخلايا الجذعية: عبّرت الخلايا الجذعية المحرضة متعددة القدرات عن مؤشرات مستضدية سطحية مماثلة لتلك الموجودة على الخلايا الجذعية الجنينية. عبّرت الخلايا الجذعية المحرضة متعددة القدرات البشرية عن المؤشرات الخاصة بالخلايا الجذعية الجنينية البشرية، بما في ذلك SSEA-3 وSSEA-4 وTRA-1-60 وTRA-1-81 وTRA-2-49/6E وNanog. عبّرت الخلايا الجذعية المحرضة متعددة القدرات للجرذان عن SSEA-1 فقط، دون SSEA-3 أو SSEA-4، على غرار الخلايا الجذعية الجنينية للجرذان.
- جينات الخلايا الجذعية: الجينات المعبر عنها في الخلايا الجذعية الجنينية غير المتمايزة، بما في ذلك Oct-3/4 و Sox2 و Nanog و GDF3 و REX1 و FGF4 و ESG1 و DPPA2 و DPPA4 و hTERT.
- نشاط التلوميراز: يعد التلوميراز ضرورياً لاستمرار انقسام الخلايا دون قيود حد هايفليك البالغ حوالي 50 انقساماً خلوياً. تُظهر الخلايا الجذعية الجنينية البشرية نشاطاً عالياً للتلوميراز للحفاظ على التجديد الذاتي والتكاثر، كما تُظهر الخلايا الجذعية المحرضة متعددة القدرات البشرية نشاطاً عالياً للتلوميراز وتُعبّر عن إنزيم النسخ العكسي للتلوميراز البشري (hTERT)، وهو مُكوّن أساسي في مركب پروتين التلوميراز.
- تعدد القدرات: كانت الخلايا الجذعية المحرضة متعددة القدرات قادرة على التمايز بطريقة مشابهة للخلايا الجذعية الجنينية إلى أنسجة متمايزة تماماً.
- التمايز العصبي: تم تحويل الخلايا الجذعية المحرضة متعددة القدرات إلى عصبونات، معبرة عن پروتينات βIII-توبولين، وهيدروكسيلاز التيروسين، وAADC، وDAT، وChAT، وLMX1B، وMAP2. قد يشير وجود الإنزيمات المرتبطة بالكاتيكولامينات إلى أن الخلايا الجذعية المحرضة متعددة القدرات، مثل الخلايا الجذعية الجنينية البشرية، قابلة للتمايز إلى عبونات دوپامينية الفعل. وقد انخفض التعبير عن الجينات المرتبطة بالخلايا الجذعية بعد التمايز.
- التمايز القلبي: تم تحويل الخلايا الجذعية المحرضة متعددة القدرات إلى خلايا عضلات قلبية التي بدأت بالنبض تلقائياً. أظهرت خلايا عضلة القلب تعبيراً عن TnTc وMEF2C وMYL2A وMYHCβ وNKX2.5. وانخفض التعبير عن الجينات المرتبطة بالخلايا الجذعية بعد التمايز.
- تكون الورم المسخي: بعد حقن الخلايا الجذعية المحرضة متعددة القدرات في فئران تعاني من نقص المناعة، تشكلت أورام مسخية تلقائياً بعد تسعة أسابيع. الأورام المسخية هي أورام متعددة السلالات تحتوي على أنسجة مشتقة من الطبقات الجرثومية الثلاث: الأديم الباطن، الأديم المتوسط، والأديم الظاهر؛ وهذا يختلف عن الأورام الأخرى التي تتكون عادةً من نوع خلوي واحد فقط. يُعد تكون الورم المسخي اختباراً هاماً لتعدد القدرات.
- الجسم الجنيني: تشكل الخلايا الجذعية الجنينية البشرية في المزارع الخلوية تلقائياً تراكيب كروية الشكل تشبه الجنين، تُسمى "الأجسام الجنينية"، وتتكون من نواة من الخلايا الجذعية الجنينية البشرية النشطة انقسامياً والمتمايزة، ومحيط من خلايا متمايزة تماماً من الطبقات الجرثومية الثلاث. كما تشكل الخلايا الجذعية المحرضة متعددة القدرات أجساماً جنينية، ولها خلايا متمايزة محيطية.
- الفئران الكيميرية: تتواجد الخلايا الجذعية الجنينية البشرية بشكل طبيعي داخل الكتلة الخلوية الداخلية (الأرومة الجنينية) للكيسات الأرومية، وتتمايز هذه الخلايا داخل الأرومة الجنينية لتكوين الجنين، بينما تتمايز قشرة الكيسة الأرومية (الأرومة المغذية) لتكوين أنسجة خارج جنينية. لا تستطيع الأرومة المغذية المجوفة تكوين جنين حي، لذلك من الضروري أن تتمايز الخلايا الجذعية الجنينية الموجودة داخل الأرومة الجنينية لتكوين الجنين. حُقنت الخلايا الجذعية المحرضة متعددة القدرات بواسطة ماصة دقيقة في الأرومة المغذية، ثم نُقلت الكيسة الأرومية إلى إناث متلقية. وهكذا، تم إنتاج صغار فئران حية كيميرية: فئران تحتوي على مشتقات الخلايا الجذعية المحرضة متعددة القدرات موزعة في جميع أنحاء أجسامها بنسبة كيميرية تتراوح بين 10 و90%.
- التكميل الرباعي الصبغي: يمكن للخلايا الجذعية المحرضة متعددة القدرات المأخوذة من أرومات ليفية جنينية للفئران، والمحقونة في أرومات جنينية رباعية الصبغيات (والتي لا يمكنها تكوين سوى أنسجة خارج جنينية)، أن تُكوّن فئراناً كاملة غير كيمرية وخصبة، على الرغم من انخفاض معدل النجاح.[41][57][58] يمكن تعزيز كفاءة إنتاج الفئران متعددة القدرات عن طريق تعريض خط الخلايا الجذعية متعددة القدرات لفترة قصيرة لپلازميد إبيسومي يشفر Sox2 و Klf4 المهندسين وراثياً (مزيج SK).[29]
- إعادة البرمجة اللاجينية
- إزالة مثيلة المحفز: المثيلة هي نقل مجموعة ميثيل إلى قاعدة دنا، وعادة ما يكون نقل مجموعة مثيل إلى جزيء سيتوسين في موقع CpG (تسلسل سيتوسين/گوانين متجاور). يؤدي انتشار مثيلة الجين إلى تعطيل التعبير الجيني، إما بمنع نشاط پروتينات التعبير، أو باستقطاب إنزيمات تعيق التعبير. وبالتالي، فإن مثيلة الجين تُكبته فعلياً بمنع نسخه. وقد لوحظت إزالة مثيلة محفزات الجينات المرتبطة بتعدد القدرات، بما في ذلك Oct-3/4 وRex1 وNanog، في الخلايا الجذعية المحرضة متعددة القدرات، مما يدل على نشاطها كمحرضات، وعلى التحريض النشط والتعبير عن الجينات المرتبطة بتعدد القدرات في هذه الخلايا.
- مثيلة الدنا الشاملة: تتشابه الخلايا الجذعية المحرضة متعددة القدرات البشرية بشكل كبير مع الخلايا الجذعية الجنينية في أنماط مثيلة السيتوسين، أكثر من أي نوع خلوي آخر. ومع ذلك، تُظهر حوالي ألف موقع اختلافات في العديد من سلالات الخلايا الجذعية المحرضة متعددة القدرات. نصف هذه المواقع يشبه سلالة الخلايا الجسدية التي اشتُقت منها الخلايا الجذعية الجنينية، أما النصف الآخر فهو خاص بالخلايا الجذعية المحرضة متعددة القدرات. كما عُثر على عشرات المناطق التي يبلغ حجمها ميگابايتات، حيث لا يعاد برمجة الخلايا الجذعية المحرضة متعددة القدرات إلى حالة الخلية الجذعية الجنينية.[59]
- إزالة مثيلة الهيستونات: الهيستونات هي پروتينات مُكثِّفة تتمركز بنيوياً في تسلسلات الدنا، ويمكن أن تؤثر على نشاطها من خلال تعديلات مختلفة متعلقة بالكروماتين. وقد أُزيلت مثيلة هيستونات H3 المرتبطة بـ Oct-3/4 وSox2 وNanog، مما يشير إلى التعبير عن هذه الجينات.
السلامة
- إن الشاغل الرئيسي فيما يتعلق بالتطبيق السريري المحتمل للخلايا الجذعية المحرضة متعددة القدرات هو ميلها لتكوين الأورام.[60] على غرار الخلايا الجذعية الجنينية، تكون الخلايا الجذعية المحرضة متعددة القدرات بسهولة أوراماً مسخية عند حقنها في فئران تعاني من نقص المناعة. وتعتبر إدارة الغذاء والدواء الأمريكية تكون الأورام المسخية عقبة رئيسية أمام الطب التجديدي القائم على الخلايا الجذعية.
- أظهرت دراسة حديثة أجريت على الفئران حول استعادة الوظائف الحركية بعد إصابات الحبل الشوكي، أنه بعد زرع الخلايا الجذعية المحرضة متعددة القدرات البشرية في الفئران، تمايزت هذه الخلايا إلى ثلاثة أنواع من الخلايا العصبية في الحبل الشوكي. حفزت هذه الخلايا إعادة نمو الحبل الشوكي المتضرر، وحافظت على عملية التغليف المياليني، وشكلت مشابك عصبية. وقد لوحظت هذه النتائج الإيجابية لأكثر من 112 يوماً بعد إصابة الحبل الشوكي، دون تكون أي أورام.[61] ومع ذلك، أظهرت دراسة متابعة أجرتها نفس المجموعة أن سلالات متميزة من الخلايا الجذعية المحرضة متعددة القدرات البشرية كونت في النهاية أوراماً.[62]
- بما أن الخلايا الجذعية المحرضة متعددة القدرات لا يمكن إنتاجها بكفاءة عالية حالياً إلا باستخدام تعديلات جينية، فمن المتوقع عموماً أن تكون أقل أماناً وأكثر قدرة على تكوين الأورام من الخلايا الجذعية الجنينية البشرية. جميع الجينات التي ثبت أنها تعزز تكوين الخلايا الجذعية المحرضة متعددة القدرات مرتبطة بالسرطان بشكل أو بآخر. بعض هذه الجينات معروفة بأنها جينات ورمية، بما في ذلك أفراد عائلة جينات Myc. مع أن حذف جين Myc يسمح بتكوين الخلايا الجذعية المحرضة متعددة القدرات، إلا أن الكفاءة تنخفض بمقدار يصل إلى 100 ضعف.
- تم إثبات طريقة غير وراثية لإنتاج الخلايا الجذعية المحرضة متعددة القدرات باستخدام الپروتينات المؤتلفة، لكن كفاءتها كانت منخفضة للغاية.[48] مع ذلك، فإن إدخال تحسينات على هذه المنهجية لزيادة كفاءتها قد يؤدي إلى إنتاج خلايا جذعية محرضة متعددة القدرات أكثر أماناً. وتُعتبر الطرق الأخرى، مثل استخدام الڤيروسات الغدانية أو الپلازميدات، أكثر أماناً بشكل عام من منهجية الڤيروسات القهقرية.
- يُعدّ اختبار قدرة الخلايا الجذعية المحرضة متعددة القدرات على تكوين الأورام بشكل مباشر، باستخدام أساليب تحاكي الطرق المستخدمة في علاجات الطب التجديدي، مجالًا هامًا للدراسات المستقبلية في هذا المجال. وتكتسب هذه الدراسات أهمية بالغة نظراً لأن الخلايا الجذعية المحرضة متعددة القدرات لا تُكوّن أوراماً مسخية فحسب، بل إن الفئران المُشتقة منها تُظهر أيضاً معدل وفيات مرتفعاً بسبب السرطان الخبيث.[63] نُشرت ورقة بحثية عام 2010 في مجلة الخلايا الجذعية تشير إلى أن الخلايا الجذعية المحرضة متعددة القدرات أكثر قدرة على تكوين أورام من الخلايا الجذعية الجنينية، مما يدعم فكرة أن سلامة الخلايا الجذعية المحرضة متعددة القدرات تشكل مصدر قلق بالغ.[64]
- برزت المخاوف بشأن قدرة الخلايا الجذعية المحرضة متعددة القدرات على إثارة استجابة مناعية في عام 2011 عندما أجرى ژو وزملاؤه دراسة تضمنت اختبار تكوين الأورام المسخية، وأظهروا أن هذه الخلايا تُنتج استجابة مناعية قوية كافية لرفضها. ومع ذلك، عندما أُجريت عملية مماثلة على خلايا جذعية جنينية مكافئة جينياً، وجد ژو وزملاؤه أوراماً مسخية، مما يشير إلى أن الجهاز المناعي يتحمل هذه الخلايا.[65] عام 2013، حاول أراكي وزملاؤه إعادة إنتاج النتيجة التي توصل إليها ژو وزملاؤه باستخدام إجراء مختلف. فقد أخذوا خلايا من كيميرا تم استنباته من مستنسخات الخلايا الجذعية المحرضة متعددة القدرات وجنين فأر، ثم زُرعت هذه الأنسجة في فئران مسانج (متطابق جينياً). وأجروا تجربة مماثلة باستخدام الخلايا الجذعية الجنينية بدلاً من مستنسخات الخلايا الجذعية المحرضة متعددة القدرات، وقارنوا النتائج. تشير النتائج إلى عدم وجود فرق يُعتد به إحصائياً في الاستجابة المناعية التي تُنتجها الخلايا الجذعية المحرضة متعددة القدرات والخلايا الجذعية الجنينية. علاوة على ذلك، أفاد أراكي وزملاؤه بوجود استجابة مناعية ضئيلة أو معدومة لكلا نوعي الخلايا.[66] وبالتالي، لم يتمكن أراكي وزملاؤه من التوصل إلى نفس النتيجة التي توصل إليها ژو وزملاؤه.
الأبحاث الطبية
لا تزال مهمة إنتاج الخلايا الجذعية الممحرضة متعددة القدرات تمثل تحدياً نظراً للمشكلات الست المذكورة أعلاه. ومن أهم المفاضلات التي يجب التغلب عليها المفاضلة بين الكفاءة والتكامل الجيني. فمعظم الطرق التي لا تعتمد على دمج الجينات المنقولة غير فعالة، بينما تواجه الطرق التي تعتمد على دمج الجينات المنقولة مشاكل إعادة البرمجة غير الكاملة وتكون الأورام، على الرغم من تجربة عدد كبير من التقنيات والأساليب. ومن الاستراتيجيات المهمة الأخرى إجراء توصيف پروتيني للخلايا الجذعية المحرضة متعددة القدرات.[58] ينبغي أن تُسفر المزيد من الدراسات والاستراتيجيات الجديدة عن حلول مثلى للتحديات الخمسة الرئيسية. وقد يسعى أحد المناهج إلى دمج المزايا الإيجابية لهذه الاستراتيجيات في تقنية فعّالة في نهاية المطاف لإعادة برمجة الخلايا إلى خلايا جذعية محرضة متعددة القدرات.
ثمة منهجية أخرى يتمثل في استخدام الخلايا الجذعية المحرضة متعددة القدرات المستخلصة من المرضى لتحديد الأدوية العلاجية القادرة على استعادة النمط الظاهري. على سبيل المثال، تُظهر سلالات الخلايا الجذعية المحرضة متعددة القدرات المستخلصة من مرضى متلازمة خلل التنسج الأديمي الظاهر (EEC)، حيث يكون الجين p63 متحوراً، التزاماً ظهارياً غير طبيعي يمكن استعادته جزئياً بواسطة مركب صغير.[67]
نمذجة الأمراض وتطوير الأدوية
من الميزات الجذابة للخلايا الجذعية المحرضة متعددة القدرات البشرية إمكانية استخلاصها من المرضى البالغين لدراسة الأساس الخلوي للأمراض البشرية. ونظرًا لقدرة هذه الخلايا على التجدد الذاتي وتعدد القدرات، فإنها تمثل مصدراً نظرياً غير محدود للخلايا المستخلصة من المرضى، والتي يمكن تحويلها إلى أي نوع من خلايا الجسم. وتكتسب هذه الميزة أهمية خاصة لأن العديد من أنواع الخلايا البشرية الأخرى المستخلصة من المرضى تتوقف عن النمو بعد بضع دورات في المزارع الخلوية المعملية. وقد أُنتجت خلايا جذعية محرضة متعددة القدرات لعلاج طيف واسع من الأمراض الوراثية البشرية، بما في ذلك اضطرابات شائعة مثل متلازمة داون ومرض الكلى متعدد الكيسات.[68][69][70] في كثير من الحالات، تُظهر الخلايا الجذعية المحرضة متعددة القدرات المشتقة من المرضى عيوباً خلوية لا تُلاحظ في الخلايا الجذعية المحرضة متعددة القدرات من الأشخاص الأصحاء، مما يوفر نظرة ثاقبة على الفسيولوجية المرضية للمرض.[71][72] عام 2012 تأسس مشروع StemBANCC، وهو مشروع تعاوني دولي، بهدف إنشاء مجموعة من خطوط الخلايا الجذعية المحرضة متعددة القدرات لفحص الأدوية لعلاج مجموعة متنوعة من الأمراض. وقد أشرفت جامعة أكسفورد على إدارة هذا المشروع، الذي جمع التمويل والموارد من 10 شركات أدوية و23 جامعة. ويهدف المشروع إلى إنشاء مكتبة تضم 1.500 خط خلوي من الخلايا الجذعية المحرضة متعددة القدرات، تُستخدم في المراحل المبكرة لاختبار الأدوية من خلال توفير بيئة تحاكي بيئة المرض البشري.[73] علاوة على ذلك، فإن الجمع بين تقنية الخلايا الجذعية المحرضة متعددة القدرات والجزيئات الصغيرة أو المؤشرات المشفرة وراثياً للجهد والكالسيوم وفر منصة واسعة النطاق وعالية الإنتاجية لفحص سلامة الأدوية القلبية الوعائية.[74][75][76][77][78]
تخليق الأعضاء
أفاد باحثون من اليابان بإثبات جدوى استخدام الخلايا الجذعية المحرضة متعددة القدرات لتخليق أعضاء بشرية لزراعتها. وقد أُستنبتت براعم كبد بشري (iPSC-LBs) من مزيج من ثلاثة أنواع مختلفة من الخلايا الجذعية: الخلايا الكبدية (لوظائف الكبد) المستخلصة من الخلايا الجذعية المحرضة متعددة القدرات؛ والخلايا الجذعية البطانية (لتكوين بطانة الأوعية الدموية) المستخلصة من دم الحبل السري؛ والخلايا الجذعية اللحمية المتوسطة (لتكوين النسيج الضام). يُتيح هذا النهج الجديد لأنواع الخلايا المختلفة تنظيم نفسها ذاتياً لتخليق عضو معقد، مُحاكياً بذلك نمو الجنين. بعد نمو براعم الكبد في المعمل لبضعة أيام، زُرعت في جرذان، حيث سرعان ما اتصل الكبد بالأوعية الدموية للمضيف واستمر في النمو. والأهم من ذلك، أنه أدى وظائف الكبد الطبيعية، بما في ذلك استقلاب الأدوية وإنتاج الپروتينات الخاصة بالكبد. ستُراقب الدراسات اللاحقة مدى بقاء العضو المزروع في جسم المضيف (قدرته على الاندماج أو تجنب الزرع) وما إذا كان سيتحول إلى أورام.[79][80]
إعادة توليد الأعضاء
عام 2021، ثبتت فعالية نهج إعادة برمجة عوامل ياماناكا القابلة للتحويل في تجدد القلب المتضرر دون تكون أورام في الجرذان، وقد نجح هذا النهج إذا تم التدخل مباشرة قبل أو بعد الإصابة بنوبة قلبية.[81] عام 2026، قامت اليابان لأول مرة بزرع خلايا قلبية مزروعة معملياً في مريض بشري.[82]
إصلاح الأنسجة
حُفزت الخلايا الدم في للحبل السري الجنيني لتصبح خلايا جذعية متعددة القدرات باستخدام الدنا الپلازميدي. وباستخدام المؤشرات السطحية للخلايا البطانية/الخلايا المحيطة بالأوعية الدموية، CD31 وCD146، حدد الباحثون "الخلايا السلفية الوعائية"، وهي خلايا جذعية وعائية عالية الجودة ومتعددة القدرات. بعد حقن الخلايا الجذعية المحرضة متعددة القدرات مباشرة في الجسم الزجاجي لشبكية العين المتضررة لدى الجرذان، اندمجت الخلايا الجذعية في الشبكية، ونمت، وأصلحت الأوعية الدموية.[83][84]
وقد تبين أن الخلايا الجذعية العصبية المشتقة من الخلايا الجذعية المحرضة متعددة القدرات والموسومة، والتي حُقنت في حيوانات العمل المصابة بآفات دماغية، تهاجر إلى الآفات، ولوحظ بعض التحسن في الوظائف الحركية.[85]
خلايا عضلة القلب
يمكن إنتاج خلايا عضلة القلب النابضة، المشتقة من الخلايا الجذعية المحرضة متعددة القدرات، بكميات كبيرة باستخدام پروتوكولات التمايز المحددة كيميائياً.[86][87] تقوم هذه الپروتوكولات عادة بتعديل نفس مسارات الإشارات التطورية المطلوبة لتطور القلب.[88] تستطيع خلايا عضلة القلب المشتقة من الخلايا الجذعية المحرضة متعددة القدرات محاكاة اضطرابات نظم القلب الوراثية واستجابات القلب للأدوية، لأنها تُظهر نفس الخلفية الجينية للمريض الذي اشتُقت منه.[89][90][91][92]
في يونيو 2014، حصلت شركة تاكارا بيو على نقل التكنولوجيا من شركة آيهارت اليابان، وهي شركة ناشئة تابعة لمعهد أبحاث الخلايا الجذعية المحرضة متعددة القدرات بجامعة كيوتو، مما مكنها من استخدام التقنيات وبراءات الاختراع التي تحرض تمايز الخلايا الجذعية المحرضة متعددة القدرات إلى خلايا عضلة القلب بشكل حصري في آسيا. وأعلنت الشركة عن فكرة بيع خلايا عضلة القلب لشركات الأدوية والجامعات للمساعدة في تطوير أدوية جديدة لأمراض القلب.[93]
في 9 مارس 2018، وافقت لجنة الطب التجديدي المتخصصة بجامعة أوساكا رسمياً على أول خطة بحثية سريرية في العالم لزراعة "صفيحة عضلية قلبية" مصنوعة من خلايا جذعية محرضة متعددة القدرات في قلب مرضى قصور القلب الحاد. وأعلنت جامعة أوساكا أنها قدمت طلباً إلى وزارة الصحة في اليوم نفسه.
في 16 مايو 2018، أُعتمدت خطة البحث السريري من قبل فريق الخبراء التابع لوزارة الصحة بشرط.[94][95]
في أكتوبر 2019، قام فريق في جامعة أوكاياما بتطوير نموذج لمرض القلب الإقفاري باستخدام خلايا عضلة القلب المتمايزة من الخلايا الجذعية المحرضة متعددة القدرات.[96]
في 19 فبراير 2026 أعلنت وزارة الصحة اليابانية يوم اخميس أن لجنة من المتخصصين قد أقرت علاج شركة سوميتومو فارما Sumitomo Pharma (4506.T) المشتق من الخلايا الجذعية المستحثة عديدة القدرات لعلاج مرض پاركنسن، مما يمهد الطريق لأول منتجات طبية في العالم تعتمد على هذه التقنية. تتمتع الخلايا الجذعية المستحثة عديدة القدرات بالقدرة على التحول إلى أنواع مختلفة من خلايا الجسم. وقد فاز العالم الياباني شنيا ياماناكا بجائزة نوبل في الطب 2012 لاكتشافه هذه الخلايا.[97]
كما اعتمدت اللجنة رقع الخلايا العضلية القلبية المشتقة من الخلايا الجذعية المستحثة من شركة كوريپس Cuorips (4894.T)، والتي تفتح أملاً جديداً لعلاج قصور القلب الحاد. وأفادت صحيفة ماينإيتشي شيمبون أنه من المتوقع أن تعتمد وزارة الصحة اليابانية هذين الدوائين في مارس 2026. بعد موافقة لجنة وزارة الصحة، يجب إعادة التحقق من سلامة الدوائين وفعاليتهما خلال سبع سنوات، وإذا كانت أنظمة التصنيع والمؤسسات الطبية جاهزة، يمكن للمرضى البدء في تلقي العلاجات بموجب التأمين الصحي العام في وقت مبكر من صيف 2026. تتكون الرقعة العلاجية من خلايا عضلية قلبية مخلقة معملياً، وتُستخدم لعلاج اعتلال عضلة القلب الإقفاري (Ischemic cardiomyopathy)، وهي حالة مرضية ينخفض فيها تدفق الدم نتيجة اعتلال عضلة القلب. وقد طُوِّرت هذه الرقعة من قِبَل شركة كوريپس الناشئة التابعة لجامعة أوساكا.
علاج مرض پاركنسن
يُسبب مرض پاركنسن تشوهات في الخلايا العصبية في المخ، مما يُؤدي إلى إصابة المرضى برعشة وصعوبة في التحكم بالحركة. في اليابان وحدها، يُقدّر عدد مرضى پاركنسن الذين ينتظرون إيجاد علاج له بنحو 300.000 مريض. يستخدم علاج شركة سوميتومو فارما خلايا مشتقة من الخلايا الجذعية المستحثة عديدة القدرات التي تنمو لتصبح خلايا عصبية. تُزرع هذه الخلايا في المخ لاستعادة وظائف الأعصاب. في التجارب السريرية، لاحظ بعض المرضى تحسناً في المهارات الحركية. يقول الباحثون أنهم تمكنوا من تأكيد سلامة العلاج وفعاليته.
خلايا الدم الحمراء
على الرغم من أن نصف لتر من الدم المتبرع به يحتوي على حوالي 2 تريليون خلية دم حمراء، ويُجمع أكثر من 107 مليون وحدة دم متبرع بها عالمياً، إلا أن الحاجة إلى الدم لنقله لا تزال قائمة. عام 2014، تم تصنيع خلايا الدم الحمراء من فصيلة O في مصلحة نقل الدم الوطنية الإسكتلندية باستخدام الخلايا الجذعية المحرضة متعددة القدرات. حُرضت هذه الخلايا لتصبح [[أديم متوسط، ثم خلايا دم، ثم خلايا دم حمراء. تمثلت الخطوة الأخيرة في جعلها تتخلص من نواتها وتنضج بشكل سليم. يمكن نقل الفصيلة O إلى جميع المرضى. لم يكن من المتوقع بدء التجارب السريرية على البشر قبل عام 2016.[98]
التجارب السريرية
أُعتمدت على أول تجربة سريرية بشرية باستخدام الخلايا الجذعية المحفرضة متعددة القدرات ذاتية الاغتراس من قبل وزارة الصحة اليابانية، وكان من المقرر إجراؤها عام 2014 في مركز رايكن لعلم الأحياء التنموي في كوبى. إلا أن التجربة عُلّقت بعد دخول قوانين الطب التجديدي الجديدة في اليابان حيز التنفيذ في نوفمبر 2015.[99] وبشكل أكثر تحديداً، تم تعزيز مجموعة من المبادئ التوجيهية الحالية لتصبح لها قوة القانون (كانت في السابق مجرد توصيات).[100] أُعيد برمجة الخلايا الجذعية المحرضة متعددة القدرات المشتقة من خلايا جلدية مأخوذة من ستة مرضى مصابين بالتنكس البقعي الرطب المرتبط بالعمر، لتتمايز إلى خلايا نسيج طلائي صبغي شبكي (RPE). ثم زُرعت هذه الخلايا في الشبكية المصابة بعد استئصال النسيج الطلائي الصبغي الشبكي المتضرر. وكان من المقرر أن تستمر مراقبة السلامة واستعادة البصر من سنة إلى ثلاث سنوات.[101][102]
في مارس 2017، أكمل فريق بقيادة ماسايو تاكاهاشي أول عملية زرع ناجحة للخلايا الشبكية المشتقة من الخلايا الجذعية المحرضة متعددة القدرات من متبرع إلى عين شخص مصاب بالتنكس البقعي المتقدم.[103] لكن ورد أن حالتهم الآن متدهورة.[104] تتمثل فوائد استخدام الخلايا الجذعية المحرضة متعددة القدرات ذاتية الانغراس في عدم وجود خطر أن يرفضها الجسم نظرياً، وفي أنها تُغني عن استخدام الخلايا الجذعية الجنينية. مع ذلك، فإن هذه الخلايا الجذعية المحرضة متعددة القدرات مُستمدة من شخص آخر.[102]
تجري حالياً تجارب سريرية جديدة تتضمن الخلايا الجذعية المحرضة متعددة القدرات ليس في اليابان فقط، لكن أيضاً في الولايات المتحدة وأوروپا.[105] أظهر بحث أُجري عام 2021 على سجل التجارب السريرية Clinicaltrials.gov وجود 129 تجربة سريرية تتضمن ذكر الخلايا الجذعية المحرضة متعددة القدرات، لكن معظمها كان غير تدخلي.[106]
استراتيجية الحصول على خلايا جذعية محرضة متعددة القدرات شاملة
لجعل تقنيات الطب التجديدي القائمة على الخلايا الجذعية المحرضة متعددة القدرات متاحة لعدد أكبر من المرضى، من الضروري ابتكار خلايا جذعية محرضة متعددة القدرات شاملة يمكن زرعها بغض النظر عن النمط الفرداني لمستضدات الكريات البيضاء البشرية (HLA). وتتمثل الاستراتيجية الحالية لابتكار هذه الخلايا في هدفين رئيسيين: إزالة التعبير عن HLA ومنع هجمات الخلايا القاتلة الطبيعية (NK) الناتجة عن حذف HLA. أُفيد أن حذف جينيّ B2M وCIITA باستخدام نظام كريسپر/كاس9 يُثبّط التعبير عن جزيئات HLA من الفئتين الأولى والثانية على التوالي. ولتجنب هجمات الخلايا القاتلة الطبيعية، استُخدمت تقنية تنبيغ الربيطات مثبطة للخلايا القاتلة الطبيعية، مثل HLA-E وCD47.[107] يُترك HLA-C دون تغيير، لأن الأليلات الـ 12 الشائعة لـ HLA-C كافية لتغطية 95% من سكان العالم.[107]
الخصائص المضادة للشيخوخة
تُبشّر الخلايا الجذعية اللحمية المتوسطة متعددة القدرات، عند تحريضها على التمايز إلى أنواع متعددة من الخلايا، بإمكانية كبيرة لإبطاء أو عكس مظاهر الشيخوخة. وقد أُثبتت هذه الخصائص المضادة للشيخوخة في تجارب سريرية مبكرة عام 2017.[108] عام 2020، خلص باحثون من جامعة ستانفورد بعد دراسة الجرذان المسنة إلى أن الخلايا البشرية القديمة عند تعرضها لعوامل ياماناكا، قد تتجدد وتصبح غير قابلة للتمييز تقريباً عن نظيراتها الأصغر سناً.[109]
الخلايا الجذعية متعددة القدرات منخفضة المناعة
استعرضت دراسة نُشرت عام 2025 تطوير الخلايا الجذعية متعددة القدرات منخفضة الاستجابة المناعية (hPSCs) باستخدام تقنيات متقدمة لتحرير الجينوم، بهدف تقليل خطر الرفض المناعي في العلاج الخلوي متغاير المنشأ. تُهندس هذه الخلايا بحيث تفتقر إلى التعبير عن جزيئات معقد التوافق النسيجي الرئيسي (MHC) من الفئتين الأولى والثانية، مع التعبير عن جينات مُعدِّلة للمناعة مثل PD-L1 وCD47 وHLA-G. يعزز هذا المزيج التهرب المناعي ويدعم مفهوم الخلايا المانحة العامة التي لا تتطلب مطابقة مستضدات الكريات البيضاء البشرية (HLA). كما يُعزز دمج أنظمة الجينات الانتحارية، مثل كاسپيز-9 المُحفَّز، السلامة بشكل أكبر من خلال تمكين الإزالة الانتقائية للخلايا في حالة الإصابة بالورم الخبيث. تهدف هذه الاستراتيجيات إلى تحسين سلامة العلاجات التجديدية وقابليتها للتوسع وسهولة الوصول إليها.[110]
انظر أيضاً
- الخلايا الجذعية المحرضة
- العلاج بالخلايا الجذعية
- اكتساب تعددية القدرات بواسطة المحرض، ادعاء تم دحضه الآن حول توليد الخلايا الجذعية متعددة القدرات عن طريق غمر الخلايا في حمض
- Dedifferentiation
- تمايز موجه
- تعدد القدرات
المصادر
- ^ أ ب ت ث Takahashi K, Yamanaka S (August 2006). "Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors". Cell. 126 (4): 663–76. doi:10.1016/j.cell.2006.07.024. hdl:2433/159777. PMID 16904174.

- ^ "The Nobel Prize in Physiology or Medicine – 2012 Press Release". Nobel Media AB. 8 October 2012.
- ^ Mahla RS (2016). "Stem Cells Applications in Regenerative Medicine and Disease Therapeutics". International Journal of Cell Biology. 2016 6940283. doi:10.1155/2016/6940283. PMC 4969512. PMID 27516776.
- ^ Klimanskaya I, Chung Y, Becker S, Lu SJ, Lanza R (November 2006). "Human embryonic stem cell lines derived from single blastomeres". Nature. 444 (7118): 481–5. Bibcode:2006Natur.444..481K. doi:10.1038/nature05142. PMID 16929302. S2CID 84792371.
- ^ Hockemeyer D, Jaenisch R (May 2016). "Induced Pluripotent Stem Cells Meet Genome Editing". Cell Stem Cell. 18 (5): 573–86. doi:10.1016/j.stem.2016.04.013. PMC 4871596. PMID 27152442.
- ^ "「i」PSなぜ小文字? 山中さんってどんな人?". 朝日新聞. 2012-10-08. Archived from the original on 21 November 2012. Retrieved 2013-04-27.
- ^ "万能なiPS細胞「iPodのように普及してほしい」". スポーツニッポン. 2012-10-09. Retrieved 2012-10-14.
- ^ "山中教授の「iPS細胞」ってiPod のパクリ!?流行らせたいと頭小文字". J-CASTニュース. 2012-10-09. Retrieved 2013-04-28.
- ^ Eguizabal C, Aran B, Chuva de Sousa Lopes SM, Geens M, Heindryckx B, Panula S, Popovic M, Vassena R, Veiga A (2019). "Two decades of embryonic stem cells: a historical overview". Human Reproduction Open. 2019 (1) hoy024. doi:10.1093/hropen/hoy024. PMC 6396646. PMID 30895264.
- ^ Yamanaka S (December 2013). "The winding road to pluripotency (Nobel Lecture)". Angewandte Chemie. 52 (52): 13900–9. Bibcode:2013ACIE...5213900Y. doi:10.1002/anie.201306721. PMID 24255017.
- ^ Guo XL, Chen JS (2015). "Research on induced pluripotent stem cells and the application in ocular tissues". International Journal of Ophthalmology. 8 (4): 818–25. doi:10.3980/j.issn.2222-3959.2015.04.31. PMC 4539634. PMID 26309885.
- ^ Thornton, Christopher D.; Fielding, Stuart; Karbowniczek, Kinga; Roig-Merino, Alicia; Burrows, Alysha E.; FitzPatrick, Lorna M.; Sharaireh, Aseel; Tite, John P.; Mole, Sara E.; Harbottle, Richard P.; Caproni, Lisa J.; McKay, Tristan R. (2021-12-10). "Safe and stable generation of induced pluripotent stem cells using doggybone DNA vectors". Molecular Therapy - Methods & Clinical Development (in English). 23: 348–358. doi:10.1016/j.omtm.2021.09.018. ISSN 2329-0501. PMC 8546411. PMID 34729381.
{{cite journal}}: CS1 maint: unrecognized language (link) - ^ Okita K, Ichisaka T, Yamanaka S (July 2007). "Generation of germline-competent induced pluripotent stem cells". Nature. 448 (7151): 313–7. Bibcode:2007Natur.448..313O. doi:10.1038/nature05934. PMID 17554338. S2CID 459050.
- ^ Wernig M, Meissner A, Foreman R, Brambrink T, Ku M, Hochedlinger K, et al. (July 2007). "In vitro reprogramming of fibroblasts into a pluripotent ES-cell-like state". Nature. 448 (7151): 318–24. Bibcode:2007Natur.448..318W. doi:10.1038/nature05944. PMID 17554336. S2CID 4377572.
- ^ Maherali N, Sridharan R, Xie W, Utikal J, Eminli S, Arnold K, et al. (June 2007). "Directly reprogrammed fibroblasts show global epigenetic remodeling and widespread tissue contribution". Cell Stem Cell. 1 (1): 55–70. doi:10.1016/j.stem.2007.05.014. PMID 18371336.
- ^ "Generations of iPSCs and related references". Archived from the original on 30 June 2018. Retrieved 5 November 2007.
- ^ Takahashi K, Tanabe K, Ohnuki M, Narita M, Ichisaka T, Tomoda K, Yamanaka S (November 2007). "Induction of pluripotent stem cells from adult human fibroblasts by defined factors". Cell. 131 (5): 861–72. doi:10.1016/j.cell.2007.11.019. hdl:2433/49782. PMID 18035408.
- ^ أ ب Yu J, Vodyanik MA, Smuga-Otto K, Antosiewicz-Bourget J, Frane JL, Tian S, et al. (December 2007). "Induced pluripotent stem cell lines derived from human somatic cells". Science. 318 (5858): 1917–20. Bibcode:2007Sci...318.1917Y. doi:10.1126/science.1151526. PMID 18029452. S2CID 86129154.
- ^ أ ب ت Yamanaka S (July 2010). "Patient-specific pluripotent stem cells become even more accessible". Cell Stem Cell. 7 (1): 1–2. doi:10.1016/j.stem.2010.06.009. PMID 20621038.
- ^ أ ب Maherali N, Hochedlinger K (December 2008). "Guidelines and techniques for the generation of induced pluripotent stem cells". Cell Stem Cell. 3 (6): 595–605. doi:10.1016/j.stem.2008.11.008. PMID 19041776.
- ^ Maherali N, Ahfeldt T, Rigamonti A, Utikal J, Cowan C, Hochedlinger K (September 2008). "A high-efficiency system for the generation and study of human induced pluripotent stem cells". Cell Stem Cell. 3 (3): 340–5. doi:10.1016/j.stem.2008.08.003. PMC 3987901. PMID 18786420.
- ^ Aasen T, Raya A, Barrero MJ, Garreta E, Consiglio A, Gonzalez F, et al. (November 2008). "Efficient and rapid generation of induced pluripotent stem cells from human keratinocytes". Nature Biotechnology. 26 (11): 1276–84. doi:10.1038/nbt.1503. PMID 18931654. S2CID 205274019.
- ^ Staerk J, Dawlaty MM, Gao Q, Maetzel D, Hanna J, Sommer CA, et al. (July 2010). "Reprogramming of human peripheral blood cells to induced pluripotent stem cells". Cell Stem Cell. 7 (1): 20–4. doi:10.1016/j.stem.2010.06.002. PMC 2917234. PMID 20621045.
- ^ Loh YH, Hartung O, Li H, Guo C, Sahalie JM, Manos PD, et al. (July 2010). "Reprogramming of T cells from human peripheral blood". Cell Stem Cell. 7 (1): 15–9. doi:10.1016/j.stem.2010.06.004. PMC 2913590. PMID 20621044.
- ^ Zhou T, Benda C, Dunzinger S, Huang Y, Ho JC, Yang J, et al. (December 2012). "Generation of human induced pluripotent stem cells from urine samples". Nature Protocols. 7 (12): 2080–9. doi:10.1038/nprot.2012.115. PMID 23138349. S2CID 205465442.
- ^ Polo JM, Liu S, Figueroa ME, Kulalert W, Eminli S, Tan KY, et al. (August 2010). "Cell type of origin influences the molecular and functional properties of mouse induced pluripotent stem cells". Nature Biotechnology. 28 (8): 848–55. doi:10.1038/nbt.1667. PMC 3148605. PMID 20644536.
- ^ Velychko S, Adachi K, Kim KP, Hou Y, MacCarthy CM, Wu G, Schöler HR (December 2019). "Excluding Oct4 from Yamanaka Cocktail Unleashes the Developmental Potential of iPSCs". Cell Stem Cell. 25 (6): 737–753.e4. doi:10.1016/j.stem.2019.10.002. PMC 6900749. PMID 31708402.
- ^ Quality of induced pluripotent stem cells is dramatically enhanced by omitting what was thought to be the most crucial reprogramming factor Oct4 is not only unnecessary but damaging during generation of mouse induced pluripotent stem cells (iPSCs)
- ^ أ ب ت MacCarthy, Caitlin M.; Wu, Guangming; Malik, Vikas; Menuchin-Lasowski, Yotam; Velychko, Taras; Keshet, Gal; Fan, Rui; Bedzhov, Ivan; Church, George M.; Jauch, Ralf; Cojocaru, Vlad; Schöler, Hans R.; Velychko, Sergiy (December 2023). "Highly cooperative chimeric super-SOX induces naive pluripotency across species". Cell Stem Cell. 31 (1): 127–147.e9. doi:10.1016/j.stem.2023.11.010. PMID 38141611.
- ^ Ali PS, Ghoshdastider U, Hoffmann J, Brutschy B, Filipek S (November 2012). "Recognition of the let-7g miRNA precursor by human Lin28B". FEBS Letters. 586 (22): 3986–90. Bibcode:2012FEBSL.586.3986S. doi:10.1016/j.febslet.2012.09.034. PMID 23063642. S2CID 28899778.
- ^ Maekawa M, Yamaguchi K, Nakamura T, Shibukawa R, Kodanaka I, Ichisaka T, et al. (June 2011). "Direct reprogramming of somatic cells is promoted by maternal transcription factor Glis1". Nature. 474 (7350): 225–9. doi:10.1038/nature10106. hdl:2433/141930. PMID 21654807. S2CID 4428172.
- ^ Luo M, Ling T, Xie W, Sun H, Zhou Y, Zhu Q, et al. (July 2013). "NuRD blocks reprogramming of mouse somatic cells into pluripotent stem cells". Stem Cells. 31 (7): 1278–86. doi:10.1002/stem.1374. hdl:10397/18487. PMID 23533168. S2CID 206512562.
- ^ Rais Y, Zviran A, Geula S, Gafni O, Chomsky E, Viukov S, et al. (October 2013). "Deterministic direct reprogramming of somatic cells to pluripotency". Nature. 502 (7469): 65–70. Bibcode:2013Natur.502...65R. doi:10.1038/nature12587. PMID 24048479. S2CID 4386833.
- ^ Selvaraj V, Plane JM, Williams AJ, Deng W (April 2010). "Switching cell fate: the remarkable rise of induced pluripotent stem cells and lineage reprogramming technologies". Trends in Biotechnology. 28 (4): 214–23. doi:10.1016/j.tibtech.2010.01.002. PMC 2843790. PMID 20149468.
- ^ أ ب Okita K, Nakagawa M, Hyenjong H, Ichisaka T, Yamanaka S (November 2008). "Generation of mouse induced pluripotent stem cells without viral vectors". Science. 322 (5903): 949–53. Bibcode:2008Sci...322..949O. doi:10.1126/science.1164270. PMID 18845712. S2CID 23735743.
- ^ Stadtfeld M, Nagaya M, Utikal J, Weir G, Hochedlinger K (November 2008). "Induced pluripotent stem cells generated without viral integration". Science. 322 (5903): 945–9. Bibcode:2008Sci...322..945S. doi:10.1126/science.1162494. PMC 3987909. PMID 18818365.
- ^ Woltjen K, Michael IP, Mohseni P, Desai R, Mileikovsky M, Hämäläinen R, et al. (April 2009). "piggyBac transposition reprograms fibroblasts to induced pluripotent stem cells". Nature. 458 (7239): 766–70. Bibcode:2009Natur.458..766W. doi:10.1038/nature07863. PMC 3758996. PMID 19252478.
- ^ Kaplan K (2009-03-06). "Cancer threat removed from stem cells, scientists say". Los Angeles Times.
- ^ Swaminathan N (2007-11-30). "Stem Cells – This Time Without the Cancer". Scientific American News. Retrieved 2007-12-11.
- ^ Marión RM, Strati K, Li H, Murga M, Blanco R, Ortega S, et al. (August 2009). "A p53-mediated DNA damage response limits reprogramming to ensure iPS cell genomic integrity". Nature. 460 (7259): 1149–53. Bibcode:2009Natur.460.1149M. doi:10.1038/nature08287. PMC 3624089. PMID 19668189.
- ^ أ ب Zhao XY, Li W, Lv Z, Liu L, Tong M, Hai T, et al. (September 2009). "iPS cells produce viable mice through tetraploid complementation". Nature. 461 (7260): 86–90. Bibcode:2009Natur.461...86Z. doi:10.1038/nature08267. PMID 19672241. S2CID 205217762.
- ^ Huangfu D, Maehr R, Guo W, Eijkelenboom A, Snitow M, Chen AE, Melton DA (July 2008). "Induction of pluripotent stem cells by defined factors is greatly improved by small-molecule compounds". Nature Biotechnology. 26 (7): 795–7. doi:10.1038/nbt1418. PMC 6334647. PMID 18568017.
- ^ أ ب Shi Y, Desponts C, Do JT, Hahm HS, Schöler HR, Ding S (November 2008). "Induction of pluripotent stem cells from mouse embryonic fibroblasts by Oct4 and Klf4 with small-molecule compounds". Cell Stem Cell. 3 (5): 568–74. doi:10.1016/j.stem.2008.10.004. PMID 18983970.
- ^ Cyranoski D (18 July 2013). "Stem cells reprogrammed using chemicals alone". Nature News. doi:10.1038/nature.2013.13416. S2CID 88247014. Retrieved 22 July 2013.
- ^ Hou P, Li Y, Zhang X, Liu C, Guan J, Li H, et al. (August 2013). "Pluripotent stem cells induced from mouse somatic cells by small-molecule compounds". Science. 341 (6146): 651–4. Bibcode:2013Sci...341..651H. doi:10.1126/science.1239278. PMID 23868920. S2CID 45685692.
- ^ "Major Step In Making Better Stem Cells From Adult Tissue". Science Daily. 19 October 2009. Retrieved 30 September 2013.
- ^ Lin T, Ambasudhan R, Yuan X, Li W, Hilcove S, Abujarour R, et al. (November 2009). "A chemical platform for improved induction of human iPSCs". Nature Methods. 6 (11): 805–8. doi:10.1038/nmeth.1393. PMC 3724527. PMID 19838168.
- ^ أ ب Zhou H, Wu S, Joo JY, Zhu S, Han DW, Lin T, et al. (May 2009). "Generation of induced pluripotent stem cells using recombinant proteins". Cell Stem Cell. 4 (5): 381–4. doi:10.1016/j.stem.2009.04.005. PMC 10182564. PMID 19398399.
- ^ Zhou W, Freed CR (November 2009). "Adenoviral gene delivery can reprogram human fibroblasts to induced pluripotent stem cells". Stem Cells. 27 (11): 2667–74. doi:10.1002/stem.201. PMID 19697349. S2CID 41418742.
- ^ David Cyranoski for Nature News. January 29, 2014 Acid bath offers easy path to stem cells
- ^ Tracy Vence for the Scientist. March 11, 2014 Call for STAP Retractions
- ^ Lies E (4 June 2014). "Japan researcher agrees to withdraw disputed stem cell paper". Reuters. Retrieved 4 June 2014.
- ^ Press Release (1 April 2014). "Report on STAP Cell Research Paper Investigation". RIKEN. Retrieved 2 June 2014.
- ^ أ ب ت Bao X, Zhu X, Liao B, Benda C, Zhuang Q, Pei D, et al. (April 2013). "MicroRNAs in somatic cell reprogramming". Current Opinion in Cell Biology. 25 (2): 208–14. doi:10.1016/j.ceb.2012.12.004. PMID 23332905.
- ^ Judson RL, Babiarz JE, Venere M, Blelloch R (May 2009). "Embryonic stem cell-specific microRNAs promote induced pluripotency". Nature Biotechnology. 27 (5): 459–61. doi:10.1038/nbt.1535. PMC 2743930. PMID 19363475.
- ^ Guenther MG, Frampton GM, Soldner F, Hockemeyer D, Mitalipova M, Jaenisch R, Young RA (August 2010). "Chromatin structure and gene expression programs of human embryonic and induced pluripotent stem cells". Cell Stem Cell. 7 (2): 249–57. doi:10.1016/j.stem.2010.06.015. PMC 3010384. PMID 20682450.
- ^ Kang L, Wang J, Zhang Y, Kou Z, Gao S (August 2009). "iPS cells can support full-term development of tetraploid blastocyst-complemented embryos". Cell Stem Cell. 5 (2): 135–8. doi:10.1016/j.stem.2009.07.001. PMID 19631602.
- ^ أ ب Boland MJ, Hazen JL, Nazor KL, Rodriguez AR, Gifford W, Martin G, et al. (September 2009). "Adult mice generated from induced pluripotent stem cells". Nature. 461 (7260): 91–4. Bibcode:2009Natur.461...91B. doi:10.1038/nature08310. PMID 19672243. S2CID 4423755.
- ^ Lister R, Pelizzola M, Kida YS, Hawkins RD, Nery JR, Hon G, et al. (March 2011). "Hotspots of aberrant epigenomic reprogramming in human induced pluripotent stem cells". Nature. 471 (7336): 68–73. Bibcode:2011Natur.471...68L. doi:10.1038/nature09798. PMC 3100360. PMID 21289626.
- ^ Knoepfler PS (May 2009). "Deconstructing stem cell tumorigenicity: a roadmap to safe regenerative medicine". Stem Cells. 27 (5): 1050–6. doi:10.1002/stem.37. PMC 2733374. PMID 19415771.
- ^ Nori S, Okada Y, Yasuda A, Tsuji O, Takahashi Y, Kobayashi Y, et al. (October 2011). "Grafted human-induced pluripotent stem-cell-derived neurospheres promote motor functional recovery after spinal cord injury in mice". Proceedings of the National Academy of Sciences of the United States of America. 108 (40): 16825–30. Bibcode:2011PNAS..10816825N. doi:10.1073/pnas.1108077108. PMC 3189018. PMID 21949375.
- ^ Nori S, Okada Y, Nishimura S, Sasaki T, Itakura G, Kobayashi Y, et al. (March 2015). "Long-term safety issues of iPSC-based cell therapy in a spinal cord injury model: oncogenic transformation with epithelial-mesenchymal transition". Stem Cell Reports. 4 (3): 360–73. doi:10.1016/j.stemcr.2015.01.006. PMC 4375796. PMID 25684226.
- ^ Aoi T, Yae K, Nakagawa M, Ichisaka T, Okita K, Takahashi K, et al. (August 2008). "Generation of pluripotent stem cells from adult mouse liver and stomach cells". Science. 321 (5889): 699–702. Bibcode:2008Sci...321..699A. doi:10.1126/science.1154884. hdl:2433/124215. PMID 18276851. S2CID 52869734.
- ^ Gutierrez-Aranda I, Ramos-Mejia V, Bueno C, Munoz-Lopez M, Real PJ, Mácia A, et al. (September 2010). "Human induced pluripotent stem cells develop teratoma more efficiently and faster than human embryonic stem cells regardless the site of injection". Stem Cells. 28 (9): 1568–70. doi:10.1002/stem.471. PMC 2996086. PMID 20641038.
- ^ Zhao T, Zhang ZN, Rong Z, Xu Y (May 2011). "Immunogenicity of induced pluripotent stem cells". Nature. 474 (7350): 212–5. CiteSeerX 10.1.1.864.8029. doi:10.1038/nature10135. PMID 21572395. S2CID 4416964.
- ^ Araki R, Uda M, Hoki Y, Sunayama M, Nakamura M, Ando S, et al. (February 2013). "Negligible immunogenicity of terminally differentiated cells derived from induced pluripotent or embryonic stem cells". Nature. 494 (7435): 100–4. Bibcode:2013Natur.494..100A. doi:10.1038/nature11807. PMID 23302801. S2CID 205232231.
- ^ Shalom-Feuerstein R, Serror L, Aberdam E, Müller FJ, van Bokhoven H, Wiman KG, et al. (February 2013). "Impaired epithelial differentiation of induced pluripotent stem cells from ectodermal dysplasia-related patients is rescued by the small compound APR-246/PRIMA-1MET". Proceedings of the National Academy of Sciences of the United States of America. 110 (6): 2152–6. Bibcode:2013PNAS..110.2152S. doi:10.1073/pnas.1201753109. PMC 3568301. PMID 23355677.
- ^ Park IH, Arora N, Huo H, Maherali N, Ahfeldt T, Shimamura A, et al. (September 2008). "Disease-specific induced pluripotent stem cells". Cell. 134 (5): 877–86. doi:10.1016/j.cell.2008.07.041. PMC 2633781. PMID 18691744.
- ^ Freedman BS, Lam AQ, Sundsbak JL, Iatrino R, Su X, Koon SJ, et al. (October 2013). "Reduced ciliary polycystin-2 in induced pluripotent stem cells from polycystic kidney disease patients with PKD1 mutations". Journal of the American Society of Nephrology. 24 (10): 1571–86. doi:10.1681/ASN.2012111089. PMC 3785271. PMID 24009235.
- ^ Dolmetsch R, Geschwind D (Jun 2011). "The human brain in a dish: the promise of iPSC-derived neurons". Cell. 145 (6): 831–4. doi:10.1016/j.cell.2011.05.034. PMC 3691069. PMID 21663789.
- ^ Grskovic M, Javaherian A, Strulovici B, Daley GQ (November 2011). "Induced pluripotent stem cells--opportunities for disease modeling and drug discovery". Nature Reviews. Drug Discovery. 10 (12): 915–29. doi:10.1038/nrd3577. PMID 22076509. S2CID 7945956.
- ^ Shi Y, Inoue H, Wu JC, Yamanaka S (Feb 2017). "Induced pluripotent stem cell technology: a decade of progress". Nat Rev Drug Discov. 16 (2): 115–30. doi:10.1038/nrd.2016.245. PMC 6416143. PMID 27980341.
- ^ Gerlin A (5 December 2012). "Roche, Pfizer, Sanofi Plan $72.7 Million Stem-Cell Bank". Bloomberg.com. Retrieved 23 December 2012.
- ^ Shinnawi R, Huber I, Maizels L, Shaheen N, Gepstein A, Arbel G, et al. (October 2015). "Monitoring Human-Induced Pluripotent Stem Cell-Derived Cardiomyocytes with Genetically Encoded Calcium and Voltage Fluorescent Reporters". Stem Cell Reports. 5 (4): 582–96. doi:10.1016/j.stemcr.2015.08.009. PMC 4624957. PMID 26372632.
- ^ Shaheen N, Shiti A, Huber I, Shinnawi R, Arbel G, Gepstein A, et al. (June 2018). "Human Induced Pluripotent Stem Cell-Derived Cardiac Cell Sheets Expressing Genetically Encoded Voltage Indicator for Pharmacological and Arrhythmia Studies". Stem Cell Reports. 10 (6): 1879–1894. doi:10.1016/j.stemcr.2018.04.006. PMC 5989818. PMID 29754959.
- ^ Sharma, Arun; Burridge, Paul W.; McKeithan, Wesley L.; Serrano, Ricardo; Shukla, Praveen; Sayed, Nazish; Churko, Jared M.; Kitani, Tomoya; Wu, Haodi; Holmström, Alexandra; Matsa, Elena (2017-02-15). "High-throughput screening of tyrosine kinase inhibitor cardiotoxicity with human induced pluripotent stem cells". Science Translational Medicine. 9 (377) eaaf2584. doi:10.1126/scitranslmed.aaf2584. ISSN 1946-6242. PMC 5409837. PMID 28202772.
- ^ McKeithan, Wesley L.; Savchenko, Alex; Yu, Michael S.; Cerignoli, Fabio; Bruyneel, Arne A. N.; Price, Jeffery H.; Colas, Alexandre R.; Miller, Evan W.; Cashman, John R.; Mercola, Mark (2017). "An Automated Platform for Assessment of Congenital and Drug-Induced Arrhythmia with hiPSC-Derived Cardiomyocytes". Frontiers in Physiology. 8 766. doi:10.3389/fphys.2017.00766. ISSN 1664-042X. PMC 5641590. PMID 29075196.
- ^ Serrano, Ricardo; Feyen, Dries A.M.; Bruyneel, Arne A.N.; Hnatiuk, Anna P.; Vu, Michelle M.; Amatya, Prashila L.; Perea-Gil, Isaac; Prado, Maricela; Seeger, Timon; Wu, Joseph C.; Karakikes, Ioannis; Mercola, Mark (January 2023). "A deep learning platform to assess drug proarrhythmia risk". Cell Stem Cell (in الإنجليزية). 30 (1): 86–95.e4. doi:10.1016/j.stem.2022.12.002. PMC 9924077. PMID 36563695.
- ^ Baker M (3 July 2013). "Miniature human liver grown in mice". Nature. doi:10.1038/nature.2013.13324. S2CID 87064973. Retrieved 19 July 2013.
- ^ Takebe T, Sekine K, Enomura M, Koike H, Kimura M, Ogaeri T, et al. (July 2013). "Vascularized and functional human liver from an iPSC-derived organ bud transplant". Nature. 499 (7459): 481–4. Bibcode:2013Natur.499..481T. doi:10.1038/nature12271. PMID 23823721. S2CID 4423004.
- ^ Chen Y, Lüttmann FF, Schoger E, Schöler HR, Zelarayán LC, Kim KP, et al. (September 2021). "Reversible reprogramming of cardiomyocytes to a fetal state drives heart regeneration in mice". Science. 373 (6562): 1537–1540. Bibcode:2021Sci...373.1537C. doi:10.1126/science.abg5159. PMID 34554778. S2CID 237617229.
- ^ Lavars, Nick (2020-01-30). "Lab-grown heart cells implanted into human patient for the first time". New Atlas (in الإنجليزية الأمريكية). Retrieved 2026-02-09.
- ^ Mullin E (28 January 2014). "Researchers repair retinas in mice with virus-free stem cells". fiercebiotech.com. Retrieved 17 February 2014.
- ^ Park TS, Bhutto I, Zimmerlin L, Huo JS, Nagaria P, Miller D, et al. (January 2014). "Vascular progenitors from cord blood-derived induced pluripotent stem cells possess augmented capacity for regenerating ischemic retinal vasculature". Circulation. 129 (3): 359–72. doi:10.1161/CIRCULATIONAHA.113.003000. PMC 4090244. PMID 24163065.
- ^ Tang H, Sha H, Sun H, Wu X, Xie L, Wang P, et al. (October 2013). "Tracking induced pluripotent stem cells-derived neural stem cells in the central nervous system of rats and monkeys". Cellular Reprogramming. 15 (5): 435–42. doi:10.1089/cell.2012.0081. PMC 3787483. PMID 24020696.
- ^ Burridge PW, Matsa E, Shukla P, Lin ZC, Churko JM, Ebert AD, et al. (August 2014). "Chemically defined generation of human cardiomyocytes". Nature Methods. 11 (8): 855–60. doi:10.1038/nmeth.2999. PMC 4169698. PMID 24930130.
- ^ Feyen, Dries A. M.; McKeithan, Wesley L.; Bruyneel, Arne A. N.; Spiering, Sean; Hörmann, Larissa; Ulmer, Bärbel; Zhang, Hui; Briganti, Francesca; Schweizer, Michaela; Hegyi, Bence; Liao, Zhandi (2020-07-21). "Metabolic Maturation Media Improve Physiological Function of Human iPSC-Derived Cardiomyocytes". Cell Reports. 32 (3) 107925. doi:10.1016/j.celrep.2020.107925. ISSN 2211-1247. PMC 7437654. PMID 32697997.
- ^ Willems E, Spiering S, Davidovics H, Lanier M, Xia Z, Dawson M, et al. (August 2011). "Small-molecule inhibitors of the Wnt pathway potently promote cardiomyocytes from human embryonic stem cell-derived mesoderm". Circulation Research. 109 (4): 360–4. doi:10.1161/CIRCRESAHA.111.249540. PMC 3327303. PMID 21737789.
- ^ Yazawa M, Hsueh B, Jia X, Pasca AM, Bernstein JA, Hallmayer J, Dolmetsch RE (March 2011). "Using induced pluripotent stem cells to investigate cardiac phenotypes in Timothy syndrome". Nature. 471 (7337): 230–4. Bibcode:2011Natur.471..230Y. doi:10.1038/nature09855. PMC 3077925. PMID 21307850.
- ^ Itzhaki I, Maizels L, Huber I, Zwi-Dantsis L, Caspi O, Winterstern A, et al. (March 2011). "Modelling the long QT syndrome with induced pluripotent stem cells". Nature. 471 (7337): 225–9. Bibcode:2011Natur.471..225I. doi:10.1038/nature09747. PMID 21240260. S2CID 4384573.
- ^ Sharma A, Burridge PW, McKeithan WL, Serrano R, Shukla P, Sayed N, et al. (February 2017). "High-throughput screening of tyrosine kinase inhibitor cardiotoxicity with human induced pluripotent stem cells". Science Translational Medicine. 9 (377) eaaf2584. doi:10.1126/scitranslmed.aaf2584. PMC 5409837. PMID 28202772.
- ^ McKeithan, Wesley L.; Feyen, Dries A. M.; Bruyneel, Arne A. N.; Okolotowicz, Karl J.; Ryan, Daniel A.; Sampson, Kevin J.; Potet, Franck; Savchenko, Alex; Gómez-Galeno, Jorge; Vu, Michelle; Serrano, Ricardo (2020-11-05). "Reengineering an Antiarrhythmic Drug Using Patient hiPSC Cardiomyocytes to Improve Therapeutic Potential and Reduce Toxicity". Cell Stem Cell. 27 (5): 813–821.e6. doi:10.1016/j.stem.2020.08.003. ISSN 1875-9777. PMC 7655512. PMID 32931730.
- ^ "iPSから心筋細胞製造 タカラバイオとベンチャー". 日本経済新聞 電子版 (in اليابانية). 24 June 2014. Retrieved 2019-11-08.
- ^ "iPSで心臓治療了承 高難度の再生医療へ一歩". 日本経済新聞 電子版 (in اليابانية). 16 May 2018. Retrieved 2019-11-08.
- ^ "iPS細胞の心筋シート移植、臨床研究を国が大筋了承:朝日新聞デジタル". 朝日新聞デジタル (in اليابانية). 16 May 2018. Archived from the original on 2019-11-08. Retrieved 2019-11-08.
- ^ Wei H, Wang C, Guo R, Takahashi K, Naruse K (December 2019). "Development of a model of ischemic heart disease using cardiomyocytes differentiated from human induced pluripotent stem cells". Biochemical and Biophysical Research Communications. 520 (3): 600–605. Bibcode:2019BBRC..520..600W. doi:10.1016/j.bbrc.2019.09.119. PMID 31623826.
- ^ "Japanese government panel endorses Sumitomo Pharma's iPS-derived treatment for Parkinson's". رويترز. 2026-02-19. Retrieved 2026-02-23.
- ^ "First transfusions of "manufactured" blood planned for 2016". Gizmag.com. 23 April 2014. Retrieved 2014-04-23.
- ^ Garber K (September 2015). "RIKEN suspends first clinical trial involving induced pluripotent stem cells". Nature Biotechnology. 33 (9): 890–1. doi:10.1038/nbt0915-890. PMID 26348942. S2CID 205271169.
- ^ Tobita M, Konomi K, Torashima Y, Kimura K, Taoka M, Kaminota M (June 2016). "Japan's challenges of translational regenerative medicine: Act on the safety of regenerative medicine". Regenerative Therapy. 4: 78–81. doi:10.1016/j.reth.2016.04.001. PMC 6581824. PMID 31245489.
- ^ Riken Center for Developmental Biology. "Information on p=roposed pilot study of the safety and feasibility of transplantation of autologous hiPSC-derived retinal pigment epithelium (RPE) cell sheets in patients with neovascular age-related macular degeneration". Research. Archived from the original on 26 June 2013. Retrieved 23 July 2013.
- ^ أ ب Gallagher J (19 July 2013). "Pioneering adult stem cell trial approved by Japan". BBC News. Retrieved 23 July 2013.
- ^ "First donor iPSC-derived RPE cell transplantation in AMD patient". RIKEN Center for Developmental Biology. 4 April 2017. Archived from the original on 6 September 2017. Retrieved 6 September 2017.
- ^ "First serious adverse reaction to iPS-derived retinal cell transplant reported". The Japan Times Online. 2018-01-17. Archived from the original on 27 January 2018. Retrieved 27 January 2018.
- ^ Deinsberger J, Reisinger D, Weber B (2020-09-11). "Global trends in clinical trials involving pluripotent stem cells: a systematic multi-database analysis". npj Regenerative Medicine. 5 (1) 15. doi:10.1038/s41536-020-00100-4. PMC 7486930. PMID 32983575.
- ^ Knoepfler P (2021-01-25). "What are induced pluripotent stem cells or IPS cells & clinical prospects?". The Niche (in الإنجليزية الأمريكية). Retrieved 2021-02-07.
- ^ أ ب Koga K, Wang B, Kaneko S (2020). "Current status and future perspectives of HLA-edited induced pluripotent stem cells". Inflammation and Regeneration. 40 23. doi:10.1186/s41232-020-00132-9. PMC 7528263. PMID 33014207.قالب:Creative Commons text attribution notice
- ^ Haridy R (23 October 2017). "Anti-Aging Stem Cell Treatment Proves Successful in Early Human Trials". New Atlas.
- ^ Sarkar TJ, Quarta M, Mukherjee S, Colville A, Paine P, Doan L, et al. (March 2020). "Transient non-integrative expression of nuclear reprogramming factors promotes multifaceted amelioration of aging in human cells". Nature Communications. 11 (1) 1545. Bibcode:2020NatCo..11.1545S. doi:10.1038/s41467-020-15174-3. PMC 7093390. PMID 32210226.
- ^ Asadi-Sarabi, Pedram; Rismani, Elham; Shabanpouremam, Mahshid; Hendi, Zahra; Nikoubin, Behnaz; Zarrabi, Ali; Vosough, Massoud (2025). "Hypoimmunogenic pluripotent stem cells: A game-changer in cell-based regenerative medicine". International Immunopharmacology. 162 115134: 115–134. doi:10.1016/j.intimp.2025.115134. PMID 40580745.
{{cite journal}}: Check|pmid=value (help)
وصلات خارجية
- Center for iPS Cell Research and Application, Kyoto University
- With few factors, adult cells take on character of embryonic stem cells
- Generating iPS Cells from MEFS through Forced Expression of Sox-2, Oct-4, c-Myc, and Klf4
- 2 Minute Video from BSCRF about Induced Pluripotent Stem Cells Archived 18 أبريل 2011 at the Wayback Machine
- 20Minute Video / The Discovery and Future of Induced Pluripotent Stem (iPS) Cells by Yamanaka January 8, 2008
- Fact sheet on reprogramming
- University of Oxford practical workshop on pluripotent stem cell technology Archived 8 أبريل 2016 at the Wayback Machine
- Allen Cell Explorer – realistic, data-driven 3D visualization of a living hiPSC in its pluri-potent state
- CamBioScience iPSC course Archived 23 أبريل 2019 at the Wayback Machine
- Induced pluripotent stem cells vs embryonic stem cells lines obtained by SCNT (discussion) on Wikiversity
- CS1 الإنجليزية الأمريكية-language sources (en-us)
- CS1 اليابانية-language sources (ja)
- CS1 errors: PMID
- Short description is different from Wikidata
- Articles with unsourced statements from May 2023
- Articles with unsourced statements from December 2012
- Articles with unsourced statements from December 2016
- Articles with hatnote templates targeting a nonexistent page
- خلايا جذعية
- خلايا جذعية محرضة
- 2006 في التكنولوجيا الحيوية